Перейти к:
Оптимизация и валидация режимов инактивации спор Bacillus subtilis в среде сверхкритического CO2: чистый газ, перекись водорода, надуксусная кислота
https://doi.org/10.47183/mes.2025-359
Аннотация
Введение. Инфекции, связанные с оказанием медицинской помощи (ИСМП), продолжают представлять существенную проблему для здравоохранения. Существующие методы стерилизации имеют ограничения по применимости к термочувствительным материалам и могут сопровождаться остаточной токсичностью или повреждением изделий. Стерилизация сверхкритическим диоксидом углерода, особенно в сочетании с окислительными добавками, представляется перспективной альтернативой, способной обеспечить требуемый уровень микробной безопасности при низких температурах и умеренных давлениях. Однако существующие данные демонстрируют значительную вариабельность результатов в зависимости от условий эксперимента, что указывает на необходимость оптимизации и валидации режимов обработки.
Цель. Оптимизация и валидация режимов стерилизации спор Bacillus subtilis в эксперименте с использованием сверхкритического диоксида углерода (scCO2), включая чистый scCO2, scCO2 с перекисью водорода (H2O2) и scCO2 с надуксусной кислотой (PAA).
Материалы и методы. Эксперименты проводили с использованием прототипа испытательного стенда для исследования режимов стерилизации. В качестве биологического индикатора использовали Bacillus subtilis subsp. spizizenii ATCC 6633 NCTC 10400. Исследование включало контаминацию титановых дисков спорами; обработку тремя режимами (чистый scCO2, scCO2 + H2O2, scCO2 + PAA); микробиологический анализ с подсчетом выживших спор; статистическую обработку результатов. Для каждого режима были реализованы центральные композиционные планы экспериментов с варьированием температуры, давления и времени экспозиции. Эффективность оценивали по показателю log-reduction жизнеспособных спор, валидационные серии включали по 10 независимых повторов.
Результаты. Газодинамическая обработка чистым scCO2 в диапазоне 35–60 °C, 70–120 атм, 60–120 мин оказалась неэффективной (максимальный log-reduction ≤ 0,8). Добавление окислителей существенно увеличивало степень инактивации: для режима scCO2 + H2O2 (200 ppm) оптимальные параметры составили 37,9 °C, 120 атм, 30 мин (log-reduction 4,4 ± 0,3; CV = 7,3%); для scCO2 + PAA (50 ppm) — 45 °C, 94 атм, 10 мин (log-reduction 6,0 ± 0,3; CV = 4,9%), что соответствует требованиям уровня гарантии стерильности (SAL) для медицинских изделий. Режим с PAA обеспечил статистически значимо более высокую эффективность по сравнению с H2O2 (t-тест, p < 0,001).
Выводы. Методика стерилизации на основе сверхкритического диоксида углерода с добавлением перекиси водорода или надуксусной кислоты обеспечивает эффективную инактивацию спор Bacillus subtilis при параметрах, соответствующих низкотемпературной обработке термочувствительных медицинских материалов, и удовлетворяет современным требованиям к стерильности медицинских изделий.
Ключевые слова
Для цитирования:
Гветадзе Р.Ш., Галстян М.С., Харах Я.Н., Колесников П.Ю., Киракосян Л.Г., Подпорин М.С., Царёв В.Н., Арутюнов С.Д. Оптимизация и валидация режимов инактивации спор Bacillus subtilis в среде сверхкритического CO2: чистый газ, перекись водорода, надуксусная кислота. Экстремальная биомедицина. 2026;28(1):134-145. https://doi.org/10.47183/mes.2025-359
For citation:
Gvetadze R.Sh., Galstyan M.S., Kharakh Ya.N., Kolesnikov P.Yu., Kirakosyan L.G., Podporin M.S., Tsarev V.N., Arutyunov S.D. Optimization and validation of Bacillus subtilis spore inactivation regimes in supercritical carbon dioxide: Pure gas, hydrogen peroxide, peracetic acid. Extreme Medicine. 2026;28(1):134-145. https://doi.org/10.47183/mes.2025-359
ВВЕДЕНИЕ
Инфекции, связанные с оказанием медицинской помощи (ИСМП), продолжают представлять существенную проблему для здравоохранения. По данным ряда публикаций, поверхности медицинских изделий могут способствовать формированию биопленок и распространению устойчивых патогенов, что осложняет профилактику и лечение ИСМП [1–3]. В ряде работ отмечается, что современные требования к безопасности и биосовместимости изделий способствуют внедрению новых материалов и усложнению конструкции, что может ограничивать применение некоторых традиционных методов стерилизации из-за потенциального риска деградации или остаточной токсичности [2][4]. Хорошо известные методы стерилизации, такие как автоклавирование, радиационное и газовое воздействие (например, оксидом этилена), имеют ограничения по применимости к термочувствительным материалам и могут приводить к остаточной токсичности или структурным изменениям изделий [4]. В связи с этим стерилизация с использованием сверхкритического диоксида углерода (scCO2) рассматривается как перспективная альтернатива благодаря сочетанию эффективности, безопасности и совместимости с современными материалами.
Для снижения риска контаминации изделий важно обеспечивать инактивацию как вегетативных, так и спорообразующих форм бактерий, включая Bacillus subtilis, который традиционно используется в качестве модельного тест-организма в исследованиях стерилизации [5–7]. В условиях расширяющихся ограничений по материалам и конструкциям устройств растет интерес к новым низкотемпературным методам, позволяющим совместить эффективность и сохранность функциональных свойств материалов. Как известно, спорообразующие бациллы, особенно B. subtilis и B. Stearothermophilus, являются наиболее устойчивыми к эрадикации представителями микромира благодаря протективным структурным особенностям их спор, поэтому являются своего рода эталонными маркерами эффективности стерилизации [5][7].
В ряде экспериментальных работ показано, что использование scCO2, а также его комбинаций с различными окислителями позволяет эффективно инактивировать споры B. subtilis при различных параметрах обработки [5–9]. Авторы большинства публикаций подчеркивают, что предлагаемые режимы стерилизации пока не являются универсальным решением, а существующие данные демонстрируют значительную вариабельность результатов в зависимости от условий эксперимента и используемых протоколов [5–7][10]. В связи с этим диапазоны поиска параметров для нашего исследования были выбраны на основании анализа литературы и технических ограничений лабораторной установки (максимальное давление 120 атм).
Цель работы — оптимизация и валидация режимов стерилизации спор Bacillus subtilis в эксперименте с использованием сверхкритического диоксида углерода (scCO2), включая чистый scCO2, scCO2 с перекисью водорода и scCO2 с надуксусной кислотой.
МАТЕРИАЛЫ И МЕТОДЫ
Экспериментальная установка
Эксперименты проводили с использованием прототипа испытательного стенда для исследования режимов стерилизации (изготовлено в «Сколковском институте науки и технологий», Россия). Установка включала рабочую камеру объемом 1 л из нержавеющей стали AISI 316 с контролем температуры от комнатной до 100 °C и максимальным рабочим давлением 120 атм. Система была оснащена программируемым логическим контроллером (ПЛК) для автоматического управления циклом, дублированным контролем давления (аналоговые манометры и цифровые датчики), а также ПИД-регулятором температуры (ТРМ210). В качестве стерилизующего агента использовали медицинский CO2. Общая схема установки представлена на рисунке 1.
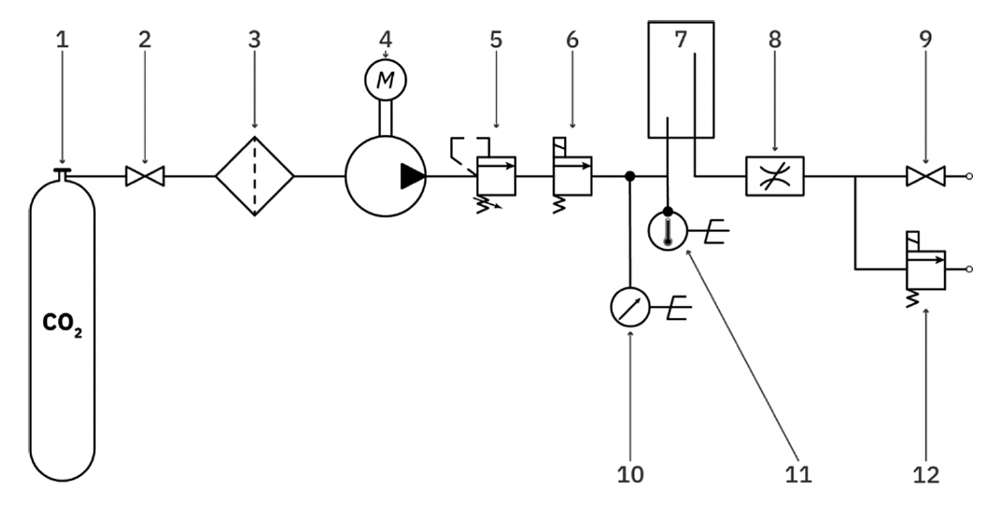
Рисунок подготовлен авторами по собственным данным
Рис. 1. Пневматическая схема прототипа испытательного стенда для исследования режимов стерилизации: 1 — баллон с газовой смесью; 2 — первый кран; 3 — фильтр; 4 — насос; 5 — клапан предохранительный; 6 — первый клапан; 7 — рабочая камера; 8 — дроссель; 9 — второй кран; 10 — электронный манометр; 11 — датчик температуры; 12 — второй клапан
Биологический индикатор
В качестве биологического индикатора использовали Bacillus subtilis subsp. spizizenii ATCC 6633 NCTC 10400.
Подготовка культуры и контаминация образцов
Для культивирования использовали питательный агар ГРМ среда № 1 следующего состава: гидролизат казеина (5,00 г/л); дрожжевой экстракт (2,50 г/л); глюкоза (1,00 г/л); агар-агар (9,00 г/л). Посевы инкубировали при температуре 37,1 °C в течение 24 ч.
Инокулюм готовили из суточной агаровой культуры, отбирая четко изолированные колонии и перенося их в стерильный 0,9% раствор натрия хлорида (NaCl) до концентрации, соответствующей 0,5 единицы стандарта мутности по Мак-Фарланду [11]. Контроль плотности взвеси проводили с помощью денситометра DEN-1 (Biosan, Латвия). Инокулюм использовали в течение 15 мин после приготовления.
На поверхность титановых дисков с помощью автоматической микропипетки наносили 100 мкл инокулюма и высушивали до полного высыхания при температуре 20 ± 2 °C в стерильных условиях. Контаминированные диски упаковывали в индивидуальные крафт-пакеты перед газодинамической обработкой (рис. 2А).

Рисунок подготовлен авторами по собственным данным
Рис. 2. Подготовка титановых дисков для газодинамической обработки: А — индивидуальная упаковка контаминированного титанового диска в крафт-пакет; Б — размещение упакованного диска в пробирке с раствором окислителя для проведения обработки по режимам CDHP или CDPAA
Микробиологический анализ
После стерилизации образцы извлекали из крафт-пакетов и помещали в стерильные контейнеры с 5 мл 0,9% раствора натрия хлорида (NaCl). Смыв проводили встряхиванием в течение 1,5 мин при 1000 об/мин с использованием вортекса V-3.
Смывную жидкость высевали в объеме 200 мкл (для скрининговых экспериментов) или 1000 мкл (для валидации экспериментов с расчетом SAL) на поверхность мясопептонного агара в чашки Петри диаметром 90 мм. Различный объем высева обусловлен методическими требованиями: для скрининговых экспериментов объем 200 мкл обеспечивал достаточную чувствительность при снижении нагрузки на автоматическую систему подсчета Scan 500; для валидационных экспериментов объем 1000 мкл максимизировал чувствительность анализа согласно ГОСТ Р ИСО1. Жидкость равномерно распределяли по поверхности среды стерильным шпателем Дригальского. Посевы инкубировали при 37 °C в течение 24 ч.
Учет результатов проводили визуально и с использованием автоматической системы подсчета колоний Scan 500 (Interscience, Франция). Для чашек, на которых получен обильный рост, учет выполняли автоматически на системе Scan 500 по методу выделенного поля: задавали область подсчета, после чего система рассчитывала плотность колоний и автоматически пересчитывала результат на всю площадь чашки с приведением к КОЕ/мл с учетом внесенного объема посева. В качестве контроля использовали образцы, не подвергавшиеся стерилизации, с которых сразу после контаминации проводили смыв аналогичным способом. Минимально детектируемое число жизнеспособных микроорганизмов (предел обнаружения методики, LOD) составляло 1 КОЕ/мл.
Подготовка химических добавок
Растворы пероксида водорода (H2O2) и надуксусной кислоты (C2H4O3) готовили в рамках научного сотрудничества с РХТУ им. Д.И. Менделеева в контролируемых условиях. Растворы готовили с использованием сверхчистой воды I типа, полученной путем двойного обратного осмоса и УФ-обработки. Все процедуры приготовления и расфасовки проводили в боксе с инертной атмосферой.
Рабочие концентрации составляли 200 ppm (0,02%) для пероксида водорода и 50 ppm (0,005%) для надуксусной кислоты.
Растворы готовили партиями с учетом срока хранения до 1 недели в условиях, рекомендованных РХТУ (при пониженной температуре без доступа света). Входной контроль исходных растворов проводили редоксиметрическими методами для уточнения концентрации.
Планирование эксперимента
С помощью статистического программного обеспечения Minitab 17.1 были сгенерированы три отдельных центральных композиционных плана (ЦКП), по одному для каждой группы обработки: CD (чистый диоксид углерода), CDHP (диоксид углерода + пероксид водорода) и CDPAA (диоксид углерода + надуксусная кислота). Для группы CD варьировали температуру в диапазоне 35–60 °C, давление 70–120 атм и время экспозиции 60–120 мин в рамках одного блока согласно данным литературы [5][7][8] с учетом технических ограничений оборудования (Pmax = 120 атм). Группы CDHP и CDPAA исследовали при температурах 30–45 °C, давлении 90–110 атм и времени экспозиции 10–30 мин согласно данным [9][12], с организацией экспериментов в 3 блока.
Каждый ЦКП включал 20 экспериментальных точек: 8 точек куба, 6 аксиальных точек и центральные точки с α = 1. Все операции с оборудованием выполнял один оператор, в то же время микробиологические процедуры проводил один специалист-микробиолог для обеспечения гомогенности получаемых данных.
Валидация оптимальных режимов стерилизации предполагала проведение серии из 10 независимых повторов для каждого режима с последующим расчетом log-reduction относительно контроля (N0). При наличии более двух моделей и соответствующих оптимальных режимов планировался сравнительный анализ значений log-reduction между группами для статистической оценки различий в эффективности стерилизации.
Экспериментальные точки выполняли согласно матрице ЦКП с контролем отклонений параметров процесса в пределах ±2 °C по температуре, ±5 атм по давлению и ±2 мин по времени экспозиции.
Экспериментальная процедура
Каждый эксперимент включал подготовку двух образцов (на матрице в виде титановых дисков размерами 8×1 мм): контрольного и тестового (экспериментального). Тест-образцы для исследования режима CD упаковывались в крафт-бумагу (рис. 2А), а для режимов CDHP и CDPAA дополнительно полностью погружались в 15 мл соответствующего раствора добавки в открытых пробирках, размещаемых в реакционной камере (рис. 2Б).
Экспериментальная процедура включала подготовку образцов и их загрузку в рабочую камеру с последующей герметизацией и достижением заданных условий по температуре и давлению CO2. После поддержания целевых условий в течение заданного времени экспозиции проводили контролируемую декомпрессию (≤10 атм/мин для минимизации эффектов механической инактивации), извлечение образцов и микробиологический анализ.
Параметры процесса (температуру, давление, время) контролировали вручную с использованием дублированных аналоговых и цифровых датчиков. Эксперименты проводили при температуре 20–25 °C и относительной влажности 50 ± 10%.
Статистический анализ
В качестве отклик-переменной используется логарифмическое снижение (log-reduction), рассчитываемое по формуле (1):
 (1)
(1)
где N0 — количество жизнеспособных микроорганизмов в контрольном образце;
N — после обработки.
Для выявления зависимости эффективности стерилизации от параметров процесса применяется методология поверхностей отклика с построением полноквадратичных моделей.
Для каждой экспериментальной группы предполагалась предварительная оценка распределения данных с использованием теста Андерсона – Дарлинга (AD). В зависимости от результата проверки нормальности для сравнения контрольных и обработанных образцов планировалось применение либо двухвыборочного t-теста (при отсутствии значимых отклонений), либо непараметрического критерия Манна – Уитни, с поправкой на совпадения (MW). Стерильность медицинских изделий считается обеспеченной при log-reduction ≥ 6, что соответствует уровню гарантии стерильности (SAL) ≤ 10⁻⁶ согласно требованиям ГОСТ2.
РЕЗУЛЬТАТЫ
Результаты для группы CD
Исходные данные и распределение отклика. В эксперименте по обработке спор Bacillus subtilis чистым CO2 было проведено 20 опытов с варьированием температурных режимов (от 35 до 60 °C), давления (от 70 до 120 атм) и времени экспозиции (от 60 до 120 мин). Среднее значение log-reduction составило 0,52 ± 0,35 (AD: p > 0,05).
DOE-анализ: полноквадратичная модель. Анализ дисперсии (ANOVA) показал отсутствие статистической значимости модели (F = 0,26; p = 0,972; R² = 19,1 %, adj R² = 0 %), только 19% изменчивости объясняется факторами (температура, давление, время экспозиции), остальные 81% обусловлены случайной ошибкой. Ни один из коэффициентов, включая основные, квадратичные и взаимодействующие члены, не был статистически значим (все p > 0,2).
Для проверки устойчивости вывода о статистической незначимости полноквадратичной модели дополнительно применяли поэтапную процедуру исключения переменных (методом обратного исключения) при α = [ 0,1; 0,3] (шаг = 0,1). Во всех случаях итоговая модель сводилась к константе, так как ни одна переменная не достигла статистической значимости (минимальное p = 0,24), а объясненная дисперсия не превышала 10%.
Статистический анализ различий между группами
В контрольной группе CD (N0) медиана числа жизнеспособных спор составила 4,34×10³ [ 2940; 5245] КОЕ/мл, в обработанной группе CD (N) — 1,57×10³ [ 556; 2678] КОЕ/мл.
Проверка нормальности распределения данных показала отсутствие отклонений от нормального закона в обработанной группе (AD: p > 0,05), однако для контрольной группы выявлено статистически значимое отклонение (AD: p < 0,05). В связи с этим для сравнения между группами применен непараметрический критерий, который выявил статистически значимое различие (MW: p < 0,001). Таким образом, снижение числа жизнеспособных спор после обработки чистым CO2 является статистически значимым.
Результаты для группы CDHP
Исходные данные и динамика расширения экспериментальной серии. В исходной серии экспериментов по обработке спор Bacillus subtilis смесью CO2 и перекиси водорода (CDHP) было выполнено 20 опытов с варьированием температуры (30–45 °C), давления (90–110 атм) и времени экспозиции (10–30 мин). Анализ построенной регрессионной модели выявил низкое значение объясненной дисперсии (R² = 45%; adj R² = 0%), все коэффициенты, включая линейные, квадратичные и взаимодействующие эффекты, оказались статистически незначимыми (p > 0,4), а тест lack-of-fit показал высокое значение (p = 0,94), что свидетельствует о неспособности модели объяснять вариацию экспериментальных данных. Процедура пошагового исключения факторов (методом обратного исключения) не позволила отобрать ни одного предиктора, а итоговая модель включала только константу.
Структура исходного экспериментального плана была несбалансированной: основная часть повторов приходилась на центральную точку (7 повторов), в то время как на экстремальных значениях факторов (давление 90 и 110 атм; время экспозиции 10 и 30 мин) было выполнено лишь по 2 эксперимента, а по ряду сочетаний факторов отсутствовали независимые повторы.
В совокупности эти результаты указывали на недостаточную информативность исходного дизайна и обосновывали необходимость целевого расширения серии. В связи с этим были добавлены пять дополнительных точек, расположенных в центральной области и на границах варьируемых факторов (табл. 3, № 21–25). В расширенной выборке (n = 25) отмечалось незначительное улучшение параметров модели (R² = 40%; adj R² =4 %), однако ключевые эффекты по-прежнему оставались незначимыми (p > 0,25 для всех факторов; lack-of-fit: p = 0,97), и процедура пошагового исключения вновь не позволила выделить статистически значимые предикторы. Для дополнительной проверки влияния давления на эффективность стерилизации были добавлены еще шесть точек с экстремальными значениями давления (70 и 120 атм, при фиксированной температуре 38 °C). Медианное значение log-reduction для полной выборки (n = 31) составило 1,31 [ 0,50; 2,61] (AD: p < 0,05).
Итоговый анализ экспериментальной серии (n = 31): модель и статистические параметры
Для определения влияния факторов на эффективность инактивации спор была построена множественная регрессионная модель с применением процедуры пошагового обратного исключения факторов (α = 0,1). В итоговую модель вошли линейные и квадратичные эффекты температуры и давления, а также линейный эффект времени экспозиции. Взаимодействия между факторами были исключены как незначимые. Регрессионное уравнение предсказанного значения log-reduction для группы CDHP (YCDHP) имеет вид:
YCDHP = 1,60 + 0,387 × tC – 0,1800 × Patm +
+ 0,01542 × Tmin – 0,00511 × tC² + 0,000996 × Patm². (2)
Объясняющая способность модели увеличилась до 58,5% (R² = 58,5%; adj R² = 50,2%; pred R² = 38,5%; lack-of-fit: p = 0,32). Статистически значимыми оказались квадратичные члены температуры (p < 0,05) и давления (p < 0,001), а также линейный эффект давления (p < 0,05), тогда как все остальные переменные были исключены на этапе отбора из-за отсутствия значимости (p > 0,1).
Статистический анализ различий между группами
В контрольной группе CDHP (N0, n = 31) медиана числа жизнеспособных спор составила 3,1×10³ [ 2950; 3680] КОЕ/мл, в обработанной группе (N, n = 31) — 1,9×10² [ 101; 474] КОЕ/мл. Проверка нормальности распределения КОЕ/мл выявила статистически значимые отклонения от нормального закона в обеих группах (AD: p < 0,005). Учитывая это, для сравнения между группами был применен непараметрический критерий, результаты которого показали статистически значимое различие между группами (MW: p < 0,0001). Наглядная демонстрация эффекта обработки приведена в сопоставлении внешнего вида контрольного и обработанного образцов (рис. 3).

Рисунок подготовлен авторами по собственным данным
Рис. 3. Пример внешнего вида чашек Петри: контрольный образец (слева) и образец после обработки по одному из исследованных режимов CDHP (справа)
Поиск оптимальных условий обработки
Для определения оптимального режима стерилизации был проведен анализ полученной регрессионной модели (YCDHP). В качестве критерия оптимальности использовалось максимальное значение log-reduction в пределах диапазона исследованных факторов (рис. 4).

Рисунок подготовлен авторами по собственным данным
Рис. 4. Поверхности отклика показателя log-reduction по регрессионной модели для группы CDHP (n = 31): А — P_atm и t_C при фиксированном T (30 мин); Б — P_atm и T_min при фиксированном t (37,9 °C); В — t_C и T_min при фиксированном P (120 атм); t_C — температура; P_atm — давление, атм; T_min — время экспозиции, мин; log_red — отклик: log10-снижение (log10-ед)
По результатам расчета определено, что максимальный эффект достигается при температуре 37,9 °C, давлении 120 атм и времени экспозиции 30 мин (рис. 5). При этих условиях предсказанное значение log-reduction составляет 2,14 (95% ДИ: [ 1,78; 2,50]; 95% ПИ (предсказательный интервал): [ 1,42; 2,87]), а интегральный критерий оптимальности (D) для найденного решения составил 0,78.

Рисунок подготовлен авторами по собственным данным
Рис. 5. График поиска оптимальных условий обработки для группы CDHP: n = 31; t_C — температура, °С; P_atm — давление, атм; T_min — время экспозиции, мин; log_red — log10-снижение; D — интегральная желательность; вертикальные линии — оптимальные уровни факторов
Диагностика модели
Диагностика финальной регрессионной модели (n = 31) осуществлена на основании визуального анализа распределения остатков. Нормальный вероятностный график (рис. 6A) показал наличие отклонения остатков от нормального закона, однако явных выбросов или структурных паттернов выявлено не было. Аналогично на графике остатков по предсказанным значениям (рис. 6Б) не выявлено систематических трендов или признаков гетероскедастичности.
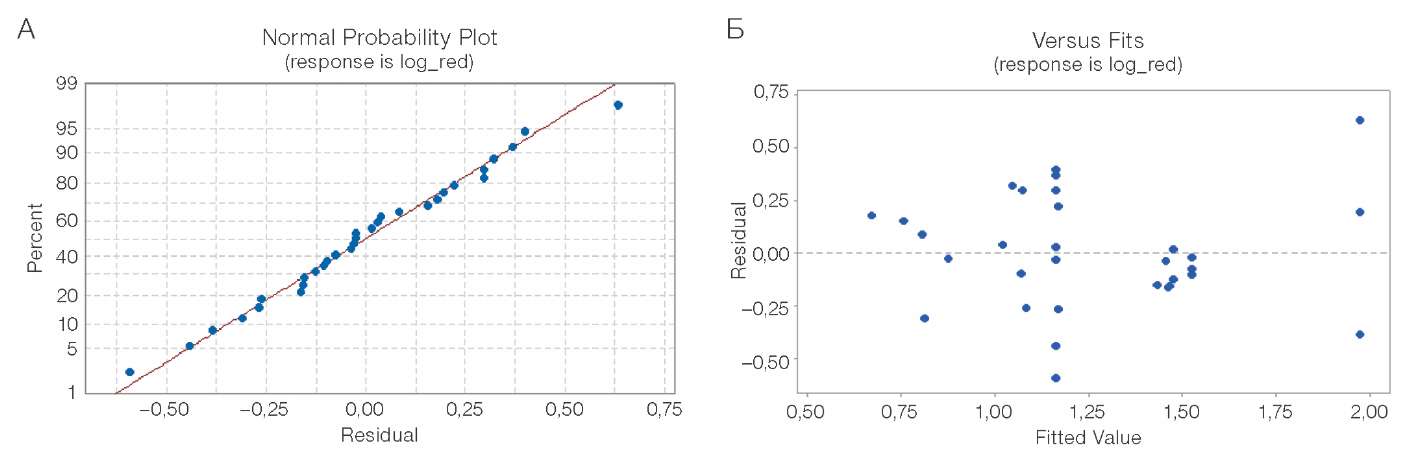
Рисунок подготовлен авторами по собственным данным
Рис. 6. Диагностика остатков модели log-reduction (группа CDHP, n = 31): А — нормальный вероятностный график (ось X: остатки, log10-ед; ось Y: процент, %); Б — график остатков по предсказанным значениям (ось X: предсказанные значения log10-снижения, log10-ед.; ось Y: остатки, log10-ед)
Результаты для группы CDPAA
Исходные данные и распределение отклика. В эксперименте по обработке спор B. subtilis смесью CO2 и надуксусной кислоты (CDPAA) было проведено 20 опытов с варьированием температуры (30–45 °C), давления (90–110 атм) и времени экспозиции (10–30 мин). Среднее значение log-reduction составило 2,10 ± 0,90 (AD: p > 0,05).
DOE-анализ: полноквадратичная модель
В отличие от предыдущих экспериментальных серий, для режима CDPAA было решено не упрощать полноквадратичную модель в связи с тем, что показатели качества данной модели оказались удовлетворительными (R² = 78,0%; adj R² = 47,6%; lack-of-fit: p = 0,08). Регрессионное уравнение предсказанного значения log-reduction для группы CDPAA (YCDPAA) имеет вид:
YCDPAA = –19,80 + 0,163 × tC + 0,387 × Patm –
– 0,106 × Tmin – 0,00219 × tC² – 0,00263 × Patm² +
+ 0,00027 × tmin² + 0,00190 × tC × Patm – (3)
– 0,00347 × tC × Tmin + 0,00207 × Patm × Tmin.
Из всех включенных в модель факторов только линейный эффект температуры оказался статистически значимым (p < 0,05), в то время как влияние давления (p > 0,05), времени экспозиции (p > 0,05), квадратичные и взаимодействующие члены не достигли статистической значимости (все p > 0,22).
Статистический анализ различий между группами
В контрольной группе CDPAA (N0, n = 20) медиана числа жизнеспособных спор составила 2,13×10³ [ 1600; 3973] КОЕ/мл, в экспериментальной группе (N, n = 20) — 2,21×10¹ [ 12,5; 41,1] КОЕ/мл (AD: p < 0,005). Статистический анализ значимости различий определил достоверное снижение числа жизнеспособных спор после обработки (MW: p < 0,0001). На рисунке 7 приведено сравнение внешнего вида контрольного и обработанного образцов.

Рисунок подготовлен авторами по собственным данным
Рис. 7. Пример внешнего вида чашек Петри: контрольный образец (слева) и образец после обработки по одному из исследованных режимов CDPAA (справа)
Поиск оптимальных условий обработки
Для определения оптимального режима стерилизации по критерию максимизации log-reduction была использована полноквадратичная модель YCDPAA (рис. 8).
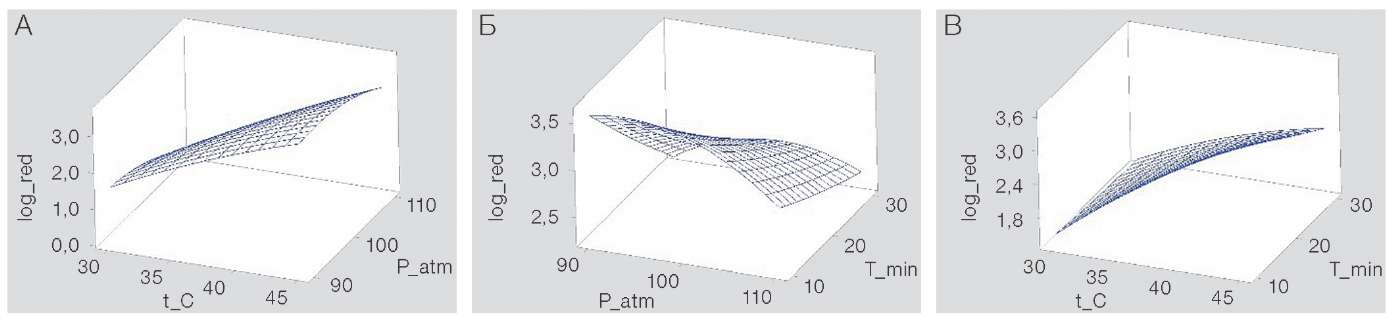
Рисунок подготовлен авторами по собственным данным
Рис. 8. Поверхности отклика показателя log-reduction по регрессионной модели для группы CDPAA: А — P_atm и t_°C при фиксированном T (10 мин); Б — P_atm и T_min при фиксированном t (45 °C); В — t_°C и T_min при фиксированном P (94 атм); t_°C — температура, °C; P_atm — давление, атм; T_min — время экспозиции, мин; log_red — отклик: log10-снижение (log10-ед)
По результатам оптимизации наивысшее ожидаемое значение log-reduction соответствует 3,60 (95% ДИ: [ 2,37; 4,82]; 95% ПИ: [ 1,65; 5,54]) и достигается при температуре 45 °C, давлении 94 атм и времени экспозиции 10 мин. Для этих условий интегральный критерий оптимальности модели составляет 0,95 (D), что указывает на высокую степень соответствия выбранного режима заданным параметрам (рис. 9).

Рисунок подготовлен авторами по собственным данным
Рис. 9. График поиска оптимальных условий обработки для группы CDPAA: t_°C — температура, °С; P_atm — давление, атм; T_min — время экспозиции, мин; log_red — log10-снижение; D — интегральная желательность; вертикальные линии — оптимальные уровни факторов
Диагностика модели
В результате оценки нормального вероятностного графика остатков (рис. 10A), а также графика остатков по предсказанным значениям (рис. 10Б) не выявлено отклонений от нормального распределения и признаков гетероскедастичности.

Рисунок подготовлен авторами по собственным данным
Рис. 10. Диагностика остатков модели log-reduction (группа CDPAA): А — нормальный вероятностный график (ось X: остатки, log10-ед; ось Y: процент, %); Б — график остатков по предсказанным значениям (ось X: предсказанные значения log10-снижения, log10-ед.; ось Y: остатки, log10-ед)
Валидация оптимальных режимов стерилизации
Для подтверждения эффективности оптимальных условий стерилизации и оценки повторяемости метода были проведены валидационные эксперименты с десятью независимыми повторами для каждого режима. В режиме CDHP (37,9 °C, 120 атм, 30 мин, 200 ppm H2O2) среднее значение log-reduction составило 4,4 ± 0,3 при коэффициенте вариации 7,3%. Для режима CDPAA (45 °C, 94 атм, 10 мин, 50 ppm PAA) среднее значение log-reduction было 6,0 ± 0,3, а коэффициент вариации — 4,9%. Во всех экспериментах значения log-reduction превышали предел обнаружения методики (1 КОЕ/мл).
Распределение данных в обеих группах соответствовало нормальному закону (AD: p > 0,05), что позволило использовать t-тест для сравнения эффективности режимов. Было установлено, что режим CDPAA обеспечивает статистически значимо более высокую инактивацию спор по сравнению с CDHP (разность средних 1,60 (log-reduction); 95% ДИ: [ 1,31; 1,89]; p < 0,001).
ОБСУЖДЕНИЕ
В ходе сравнительной оценки стерилизующего действия сверхкритического CO2 и его комбинаций с окислителями в отношении спор B. subtilis установлено, что применение только CO2 (режим CD) не позволило добиться значимого снижения жизнеспособности: во всех протестированных сочетаниях параметров уровень инактивации не превышал 0,8 log-порядка. Введение окислителей — перекиси водорода (CDHP) и надуксусной кислоты (CDPAA) — обеспечило принципиально иной результат. По данным валидационных серий, для режима CDHP среднее снижение составило 4,42 ± 0,32 log-порядка (CV = 7,30%) при 37,9 °C, 120 атм, 30 мин, а для CDPAA — 6,02 ± 0,30 log-порядка (CV = 4,98%) при 45 °C, 94 атм, 10 мин.
Коэффициенты вариации рассчитаны по серии из десяти независимых повторов для режимов с окислителями; для режима CD отдельные валидационные эксперименты не проводились, поскольку оптимальных условий, обеспечивающих высокую степень инактивации, выявить не удалось.
Достигнутое в настоящем исследовании снижение числа жизнеспособных спор B. subtilis на четыре порядка и более при обработке с использованием scCO2 и перекиси водорода указывает на потенциал этого подхода для решения задач высокоуровневой дезинфекции полукритических медицинских изделий [1][13]. Такой уровень инактивации рассматривается в современных международных рекомендациях как приемлемый для обеспечения микробиологической безопасности изделий, для которых достижение абсолютной стерильности не требуется, однако необходима эффективная защита от большинства патогенов [13–15]. Следует подчеркнуть, что в данной работе оценивали в первую очередь инактивацию спор, поэтому для практического внедрения метода необходим дальнейший анализ антимикробной активности в отношении других клинически значимых микроорганизмов.
Низкая эффективность стерилизации спор Bacillus subtilis чистым CO2, наблюдаемая в изученном диапазоне температур (35–60 °C), давлении (70–120 атм) и времени экспозиции (1–2 ч), полностью согласуется с результатами ряда независимых исследований. В работе S. Spilimbergo и соавт. [5] при 36 °C, 80 атм и длительной экспозиции (до 48 ч) log-reduction для спор B. subtilis составлял 0,5–0,9, что сопоставимо с нашими значениями 0,4–0,8 при существенно более коротком времени обработки. A.K. Dillow и соавт. [16] показали, что при 205 бар (~200 атм), 34 °C и экспозиции 2 ч для спор Bacillus cereus показатель log-reduction не превышал 1–2 у.е.; только при 60 °C и увеличении времени до 4 ч удавалось достичь log- reduction 5–8 у.е., что выходит за рамки большинства применимых для медицинских изделий режимов. А. White и соавт. [17] подтвердили, что даже при 96–103 атм и 35–60 °C log-reduction спор B. subtilis и B. stearothermophilus оставался близким к нулю даже за 72 ч; значимая инактивация наблюдалась только при добавлении окислителей или воды.
Совокупность этих данных подтверждает, что стерилизация спор чистым CO2 неэффективна при «мягких» и средних режимах, а переход к практическим уровням инактивации требует либо экстремального повышения температуры, либо значительного увеличения времени обработки, что зачастую невозможно или экономически неоправданно при работе с медицинскими материалами. Диапазон параметров был выбран исходя из ограничений экспериментальной установки и задач, связанных с применением метода к обработке медицинских изделий, что соответствует реальным условиям производства и перспективам последующего внедрения технологии.
Совпадение полученных нами значений log-reduction с диапазонами, опубликованными в ряде независимых исследований для спор Bacillus spp. при аналогичных условиях [5][16][17], может указывать на определенную воспроизводимость эффекта низкой эффективности чистого CO2 в изученных режимах. Несмотря на различия в экспериментальных моделях, объектах и деталях протоколов, значимых расхождений в достигнутом уровне инактивации не отмечено. Тем не менее для окончательных выводов о воспроизводимости требуются специально спланированные межлабораторные исследования с контролем критичных параметров.
Следует отметить, что нам не удалось выявить в литературе другие публикации об использовании штамма B. subtilis и сопоставимых условий обработки (200 ppm H2O2, температура, давление), за исключением работы V. Warambourg и соавт. [6], на параметры которой мы ориентировались при планировании собственных экспериментов. В нашем исследовании оптимальные параметры процесса (120 бар, 37,9 °C, 30 мин, 200 ppm H2O2) отличались от условий, описанных у V. Warambourg и соавт. [6] (110 бар, 40 °C, 20 мин, 200 ppm H2O2), однако находились в близком диапазоне. Совпадение диапазонов оптимальных условий, определенных независимо, может рассматриваться как проявление частичной воспроизводимости «оптимального окна» стерилизации scCO2 с H2O2 для B. subtilis. Вместе с тем достигнутые значения log-reduction существенно различаются (4,42 против 8,73), что указывает на ограничения количественной воспроизводимости между разными лабораториями и подчеркивает важность стандартизации экспериментальных методик и объектов.
В части применения CDPAA наиболее близкими по условиям к настоящему исследованию являются эксперименты B. Setlow и соавт., где для B. subtilis при 35–55 ppm PAA, 35 °C, 100 бар и времени экспозиции 25 мин наблюдали снижение жизнеспособности более чем на 6 log-порядков [12]. В нашем исследовании оптимальные параметры составили 45 °C, 94 бар, 10 мин, 50 ppm PAA. Таким образом, диапазоны концентраций, давления и температуры, при которых достигается выраженная инактивация, оказались близкими, однако различия во времени экспозиции и деталях протокола не позволяют говорить о воспроизводимости в строгом смысле и затрудняют прямое количественное сопоставление эффективности.
Несмотря на частичное совпадение ключевых параметров с опубликованными работами, корректное количественное сопоставление эффективности затруднено. Основные причины обусловлены различиями в используемых штаммах, геометрии и материале подложки, способе и объеме нанесения инокулюма, процедуре смыва, а также деталях экспериментальных протоколов. Такая вариабельность подчеркивает необходимость дальнейшей стандартизации и межлабораторного согласования ключевых параметров исследований по scCO2-стерилизации.
Доступные литературные данные по инактивации спор с использованием scCO2 в сочетании с окислителями (перекись водорода, надуксусная кислота) чрезвычайно разнородны. В большинстве публикаций изучаются различные штаммы Bacillus (чаще всего B. atrophaeus, B. pumilus, G. stearothermophilus), применяются существенно отличные концентрации окислителей и различные экспериментальные протоколы [18]. Работ, в которых бы одновременно использовались низкие концентрации окислителей, условия, сопоставимые с настоящим исследованием по температуре и давлению, а также B. subtilis в качестве тест-организма, нам выявить не удалось. Такая разрозненность и отсутствие стандартизации затрудняют корректное количественное сравнение эффективности между результатами настоящей работы и большинством опубликованных данных. Необходимость дальнейших исследований с использованием идентичных биологических объектов и согласованных режимов подчеркивается в ряде современных обзоров [12][18].
Анализ вклада отдельных факторов показал, что в режиме CDHP давление оказывало высокозначимое влияние как в линейном (p < 0,05), так и в квадратичном (p < 0,001) выражении, причем квадратичный эффект был наиболее выражен. В режиме CDPAA линейный эффект давления не достиг статистической значимости (p > 0,226), что, вероятно, связано не только с различиями в химических свойствах окислителей, но и с особенностями матрицы и локальной доступности стерилизующего агента [9]. Полученные нами данные частично согласуются с данными M.S. Hossain и соавт., где давление было определяющим фактором для инактивации бактерий в условиях обработки чистым scCO2, однако в этой работе изучались преимущественно вегетативные формы, а не споры [8]. По данным J. Zhang и соавт., давление усиливает растворимость и проникновение CO2 через клеточные барьеры, но для спор эффективность этого процесса может существенно различаться [7][9].
Температура продемонстрировала устойчивую значимость в обеих моделях: для CDHP — как линейный (p < 0,01) и квадратичный (p < 0,05) эффект, для CDPAA — как доминирующий линейный фактор (p < 0,05). Это подчеркивает ведущую роль температуры при добавлении окислителей для преодоления споровых барьеров. Значимость температурного фактора, выявленная в нашем исследовании для режима с надуксусной кислотой, согласуется с данными J. Zhang и соавт., согласно которым повышение температуры увеличивает диффузию CO2 и текучесть клеточных структур [7].
Время экспозиции оказалось статистически значимым только для CDHP (p < 0,05), но не для CDPAA (p > 0,407), что также согласуется с литературными данными о сравнительно меньшем вкладе продолжительности воздействия по сравнению с давлением и температурой [7][9]. Более быстрое действие надуксусной кислоты может объяснять снижение зависимости от времени экспозиции.
Взаимодействие давления и температуры было статистически значимым для обоих режимов (CDHP: p < 0,05; CDPAA: p < 0,05), что указывает на синергетический эффект параметров. По-видимому, на давлениях выше критического для CO2 диффузия определяется именно давлением, а повышение температуры дополнительно увеличивает текучесть оболочек и активирует окислительные процессы [7][8].
В настоящем исследовании резкая декомпрессия после обработки намеренно была исключена, чтобы минимизировать вклад механического повреждения спор и получить более объективную оценку химического действия scCO2 и окислителей. Этот подход обоснован результатами ряда работ, в которых показано, что резкая декомпрессия может вносить существенный вклад в инактивацию за счет физических эффектов, не связанных с действием самого агента [5][7][8]. По нашему мнению, такой подход позволяет получить более достоверные данные о механизмах инактивации.
Результаты валидационных экспериментов показали значения log-reduction, существенно превышающие верхние границы предсказательных интервалов, рассчитанных по основной серии при поисках оптимальных режимов. Это связано не только с применением оптимальных режимов, но и с тем, что в обеих сериях использовались разные микробиологические подходы: при построении модели исходная концентрация спор была ниже (для стабильной работы автоматического счетчика), тогда как валидация проводилась при нормативной нагрузке (N0 ≥ 10⁶), необходимой для расчета SAL [14][15].
Представленное исследование имеет ряд ограничений, которые следует учитывать при интерпретации и практическом использовании полученных данных. Работа выполнена на одной лабораторной установке с максимальным давлением 120 атм, что ограничивает диапазон исследованных режимов; эксперименты проведены только с одним модельным организмом (Bacillus subtilis subsp. spizizenii ATCC 6633) и на титановых дисках, поэтому эффективность метода для других микроорганизмов и материалов не оценивалась. Повторяемость результатов определялась только в условиях одной лаборатории, а межлабораторная воспроизводимость не изучалась. Влияние стерилизации на функциональные свойства и биосовместимость медицинских изделий также не исследовалось. Все эти ограничения следует учитывать при планировании дальнейших работ и переносе лабораторных результатов в практику.
ЗАКЛЮЧЕНИЕ
В ходе проведенных экспериментальных исследований с использованием сверхкритического диоксида углерода (scCO2), включая чистый scCO2, scCO2 с перекисью водорода (H2O2) и scCO2 с надуксусной кислотой (PAA), были валидированы режимы инактивации спор Bacillus subtilis на титановых дисках. Экспериментально обоснованы оптимальные условия для низкотемпературной обработки термочувствительных медицинских материалов, соответствующие современным международным требованиям. Режим scCO2 с надуксусной кислотой обеспечивает достижение уровня SAL ≤ 10⁻⁶, необходимого для стерилизации медицинских изделий. Режим scCO2 с перекисью водорода обеспечивает превышение SAL ≤ 10⁻⁴, что соответствует высокоуровневой дезинфекции. Использование только чистого scCO2 оказалось недостаточно эффективным (максимум 0,8 log-reduction).
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Наибольший вклад распределен следующим образом: Р.Ш. Гветадзе — административное руководство проектом, рецензирование и редактирование рукописи; М.С. Галстян — проведение экспериментов на установке, обработка первичных данных, написание первоначального варианта статьи, подготовка иллюстративного материала; Я.Н. Харах — разработка статистического дизайна исследования, статистический анализ и интерпретация результатов; П.Ю. Колесников — выполнение микробиологических исследований, культивирование микроорганизмов, проведение микробиологического анализа; Л.Г. Киракосян — техническое обеспечение экспериментов, проведение валидационных экспериментов, написание разделов методологии и результатов; М.С. Подпорин — планирование экспериментов по оптимизации режимов, научно-методическое сопровождение; В.Н. Царев — концепция микробиологической части исследования, предоставление лабораторных ресурсов, научное редактирование; С.Д. Арутюнов — концептуализация исследования, разработка методологии, утверждение окончательной версии рукописи для публикации.
1. ГОСТ Р ИСО 14937-2012 (ISO 14937:2009). Стерилизация медицинской продукции. Общие требования к определению характеристик стерилизующего агента и к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий. М.: Стандартинформ; 2013.
2. ГОСТ Р ИСО 14937-2012 (ISO 14937:2009). Стерилизация медицинской продукции. Общие требования к определению характеристик стерилизующего агента и к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий. М.: Стандартинформ; 2013.
Список литературы
1. Rowan NJ, Kremer T, McDonnell G. A review of Spaulding’s classification system for effective cleaning, disinfection and sterilization of reusable medical devices: viewed through a modern-day lens that will inform and enable future sustainability. Science of the Total Environment. 2023;878:162976. https://doi.org/10.1016/j.scitotenv.2023.162976
2. Spaulding AB, Watson D, Dreyfus J, Heaton P, Grapentine S, Bendel-Stenzel E, et al. Epidemiology of bloodstream infections in hospitalized children in the United States, 2009– 2016. Clinical Infect Diseases. 2019;69(6):995–1002. https://doi.org/10.1093/cid/ciy1030
3. Stewart S, Robertson C, Pan J, Kennedy S, Dancer S, Haahr L, et al. Epidemiology of healthcare-associated infection reported from a hospital-wide incidence study: considerations for infection prevention and control planning. Journal of Hospital Infection Society. 2021;114:10–22. https://doi.org/10.1016/j.jhin.2021.03.031
4. Арутюнов СД, Янушевич ОО, Корсунский АМ, Подпорин МС, Салимон АИ, Романенко ИИ и др. Сравнительный анализ эффективности современных методов стерилизации инструментов и место газоводинамической обработки диоксидом углерода. Российская стоматология. 2022;15(1):12–9. https://doi.org/10.17116/rosstomat20221501112
5. Spilimbergo S, Bertucco A, Lauro FM, Bertoloni G. Inactivation of Bacillus subtilis spores by supercritical CO<sub>2</sub> treatment. Innovative Food Science and Emerging Technologies. 2003;4(2):161–5. https://doi.org/10.1016/S1466-8564(02)00089-9
6. Warambourg V, Mouahid A, Crampon C, Galinier A, Claeys-Bruno M, Badens E. Supercritical CO<sub>2</sub> sterilization under low temperature and pressure conditions. The Journal of Supercritical Fluids. 2023;203:106084. https://doi.org/10.1016/j.supflu.2023.106084
7. Zhang J, Davis TA, Matthews MA, Drews MJ, LaBerge M, An YH. Sterilization using high-pressure carbon dioxide. The Journal of Supercritical Fluids. 2006;38(3):354–72. https://doi.org/10.1016/j.supflu.2005.05.005
8. Hossain MS, Nik Ab Rahman NN, Balakrishnan V, Alkarkhi AFM, Rajion ZA, Ab Kadir MO. Optimizing supercritical carbon dioxide in the inactivation of bacteria in clinical solid waste by using response surface methodology. Waste Management. 2015;43:402–9. https://doi.org/10.1016/j.wasman.2015.01.003
9. Qiu QQ, Leamy P, Brittingham J, Pomerleau J, Kabaria N, Connor J. Inactivation of bacterial spores and viruses in biological material using supercritical carbon dioxide with sterilant. Journal of Biomedical Materials Research B Applied Biomaterials. 2009;91B(2):572–8. https://doi.org/10.1002/jbm.b.31431
10. Salimon AI, Statnik ES, Kan Y, Yanushevich OO, Tsarev VN, Podporin MS, et al. Comparative study of biomaterial surface modification due to subcritical CO<sub>2</sub> and autoclave disinfection treatments. The Journal of Supercritical Fluids. 2022;191:105789. https://doi.org/10.1016/j.supflu.2022.105789
11. McFarland J. The nephelometer: an instrument for estimating the number of bacteria in suspensions used for calculating the opsonic index and for vaccines. JAMA. 1907;49(14):1176–8. https://doi.org/10.1001/jama.1907.25320140022001f
12. Setlow B, Korza G, Blatt KMS, Fey JP, Setlow P. Mechanism of Bacillus subtilis spore inactivation by and resistance to supercritical CO<sub>2</sub> plus peracetic acid. Journal of Applied Microbiology. 2016;120(1):57–69. https://doi.org/10.1111/jam.12995
13. von Woedtke T, Kramer A. The limits of sterility assurance. GMS Krankenhhyg Interdiszip. 2008;3(3):Doc19.
14. Rutala WA, Weber DJ. Sterilization, high-level disinfection, and environmental cleaning. Infectious Disease Clinics of North America. 2011;25(1):45–76. https://doi.org/10.1016/j.idc.2010.11.009
15. Shenoy ES, Weber DJ, McMullen K, Rubin Z, Sampathkumar P, Schaffzin JK, et al. Multisociety guidance for sterilization and high-level disinfection. Infection Control Hospital Epidemiology. 2025. https://doi.org/10.1017/ice.2025.41
16. Dillow AK, Dehghani F, Hrkach JS, Foster NR, Langer R. Bacterial inactivation by using near- and supercritical carbon dioxide. PNAS. 1999;96(18):10344–8. https://doi.org/10.1073/pnas.96.18.10344
17. White A, Burns D, Christensen TW. Effective terminal sterilization using supercritical carbon dioxide. Journal of Biotechnology. 2006;123(4):504–15. https://doi.org/10.1016/j.jbiotec.2005.12.033
18. Soares GC, Learmonth DA, Vallejo MC, Davila SP, González P, Sousa RA, et al. Supercritical CO<sub>2</sub> technology: The next standard sterilization technique? Material Science and Engineering: C. 2019;99:520–40. https://doi.org/10.1016/j.msec.2019.01.121
Об авторах
Р. Ш. ГветадзеРоссия
Гветадзе Рамаз Шалвович, д-р мед. наук, профессор, академик РАН
Москва
М. С. Галстян
Россия
Галстян Мариам Сережевна
Москва
Я. Н. Харах
Россия
Харах Ясер Насерович, канд. мед. наук
Москва
П. Ю. Колесников
Россия
Колесников Петр Юрьевич
Москва
Л. Г. Киракосян
Россия
Киракосян Левон Гамлетович, канд. мед. наук
Москва
М. С. Подпорин
Россия
Подпорин Михаил Сергеевич, канд. мед. наук
Москва
В. Н. Царёв
Россия
Царев Виктор Николаевич, д-р мед. наук, профессор
Москва
С. Д. Арутюнов
Россия
Арутюнов Сергей Дарчоевич, д-р мед. наук, профессор
Москва
Рецензия
Для цитирования:
Гветадзе Р.Ш., Галстян М.С., Харах Я.Н., Колесников П.Ю., Киракосян Л.Г., Подпорин М.С., Царёв В.Н., Арутюнов С.Д. Оптимизация и валидация режимов инактивации спор Bacillus subtilis в среде сверхкритического CO2: чистый газ, перекись водорода, надуксусная кислота. Экстремальная биомедицина. 2026;28(1):134-145. https://doi.org/10.47183/mes.2025-359
For citation:
Gvetadze R.Sh., Galstyan M.S., Kharakh Ya.N., Kolesnikov P.Yu., Kirakosyan L.G., Podporin M.S., Tsarev V.N., Arutyunov S.D. Optimization and validation of Bacillus subtilis spore inactivation regimes in supercritical carbon dioxide: Pure gas, hydrogen peroxide, peracetic acid. Extreme Medicine. 2026;28(1):134-145. https://doi.org/10.47183/mes.2025-359
JATS XML
















