Перейти к:
Аллельные варианты цитохромов CYP2C9, CYP2C19, CYP2D6 у жителей России: распространенность и региональное распределение
https://doi.org/10.47183/mes.2025-371
Аннотация
Введение. Определение генотипа CYP2C9, CYP2C19, CYP2D6 позволяет персонализировать терапию для широкого круга лекарственных средств. Доступные в настоящий момент диагностические панели и международные рекомендации, регламентирующие объем тестирования, базируются на общемировых данных об аллельном полиморфизме этих генов.
Цель. Определение распределения аллельных вариантов генов CYP2C9, CYP2C19 и CYP2D6 в популяции жителей РФ с учетом региональных особенностей.
Материалы и методы. Исследование выполнено на выборке из базы данных популяционных частот (GBD) ЦСП ФМБА России (n = 121 442, охват 85 субъектов РФ). Всем участникам выполнено полногеномное секвенирование ДНК, установление генотипа CYP2C9, CYP2C19 и CYP2D6 при помощи программного обеспечения PAnno. В регионах с достаточным количеством наблюдений сопоставляли частоты вариантов и доли различных фенотипов метаболизма с выделением регионов риска и регионов с аллельной структурой, отличающейся от популяционной.
Результаты. Распространенность замедленного метаболизма субстратов CYP2C9 в популяции оценивается в 33,66%, CYP2C19 — в 25,37%, CYP2D6 — в 8,29%, ускоренного метаболизма субстратов CYP2C19 — в 37,37%. К регионам риска наличия замедленного метаболизма субстратов хотя бы одного из исследуемых изоферментов относятся Чеченская Республика, Дагестан, Ингушетия, Кабардино-Балкария, Северная Осетия, Ростовская область, Чувашия, Марий Эл, Удмуртская Республика, Татарстан, Тыва, Якутия, Калмыкия, Бурятия, Карелия, Сахалинская, Иркутская и Новосибирская области. Данный риск реализуется как за счет количественных различий во встречаемости частых аллельных вариантов, так и за счет представленности в отдельных регионах редких аллелей, таких как CYP2C9*29, CYP2C9*12, CYP2C19*8, CYP2D6*32, CYP2D6*7.
Выводы. Полученные результаты создают предпосылки для разработки отечественных диагностических панелей, а также для дифференцированного подхода к фармакогенетическому тестированию в разных биогеографических группах внутри страны, внедрение которых должно сопровождаться клинико-экономическим обоснованием для каждого препарата, чья эффективность или безопасность существенно зависят от генотипа CYP2C9, CYP2C19 и CYP2D6.
Для цитирования:
Юдин В.С., Спектор Е.Д., Мамчур А.А., Иванов М.В., Митрофанов С.И., Кузьмина Л.П., Бухтияров И.В., Кескинов А.А., Юдин С.М., Каштанова Д.А. Аллельные варианты цитохромов CYP2C9, CYP2C19, CYP2D6 у жителей России: распространенность и региональное распределение. Экстремальная биомедицина. 2026;28(1):37-50. https://doi.org/10.47183/mes.2025-371
For citation:
Yudin V.S., Spektor E.D., Mamchur A.A., Ivanov M.V., Mitrofanov S.I., Kuzmina L.P., Bukhtiyarov I.V., Keskinov A.A., Yudin S.M., Kashtanova D.A. Allelic variants of CYP2C9, CYP2C19, CYP2D6 cytochromes in the Russian population: Prevalence and regional distribution. Extreme Medicine. 2026;28(1):37-50. https://doi.org/10.47183/mes.2025-371
ВВЕДЕНИЕ
Определение генотипа ферментов биотрансформации лекарственных препаратов (ЛП), среди которых значительную часть составляют изоферменты цитохрома P450, играет важную роль в персонализации лекарственной терапии. Показано, что среди популяции европейского происхождения 96,8% лиц являются носителями как минимум одного генетического варианта изоферментов цитохрома Р450, способного влиять на метаболизм лекарственных препаратов [1]. Изоферменты CYP2C9, CYP2C19, CYP2D6 ответственны за метаболизм до 45% ЛП, подвергаемых биотрансформации [2], и входят в число так называемых наиболее важных фармакогенов (very important pharmacogenes, VIP) [3].
Изофермент цитохрома CYP2C9, составляющий около 20% всех изоферментов Р450 [4], осуществляет метаболизм лекарственных препаратов, таких как варфарин и другие антикоагулянты кумариновой группы, фенитоин, флувастатин, торасемид, некоторые сартаны, пероральные сахароснижающие средства (в первую очередь производные сульфанилмочевины) и нестероидные противовоспалительные препараты (НПВП), а также значительного числа веществ эндогенного происхождения и нефармакологических ксенобиотиков [5]. Аллельные варианты CYP2C9*2 и CYP2C9*3 являются наиболее изученными и распространенными в популяции европейского происхождения [6]; данные об аллельном распределении в других популяциях активно накапливаются, демонстрируя специфику отдельных биогеографических групп.
Другой важный в фармакогенетическом аспекте изофермент, CYP2C19, является ключевым ферментом биотрансформации клопидогрела, ингибиторов протонной помпы, вориконазола, некоторых бензодиазепинов, антидепрессантов из группы селективных ингибиторов обратного захвата серотонина и трициклических антидепрессантов [7]. Варианты CYP2C19*2 и CYP2C19*3 соответствуют отсутствующей ферментной активности, что влечет за собой снижение скорости биотрансформации субстратов. Носительство аллели CYP2C19*17, напротив, сопряжено с увеличением ферментной активности и скорости метаболизма ЛП [7]. В европейской популяции, помимо дикого варианта CYP2C19*1, с достаточно высокой частотой (>1%) встречаются только варианты *2 и *17, аллель CYP2C19*3 встречается в основном в восточноазиатской популяции, а для лиц африканского происхождения характерно значительное аллельное разнообразие этого фермента с представленностью вариантов *9, *13, *15, *27 [6].
Другой изофермент, CYP2D6, имеет наибольший охват ЛП и является наиболее полиморфным. В PharmGKB приводится свыше 180 аллельных вариантов, значительная часть из которых не аннотирована либо имеет аннотацию с неизвестной/неопределенной функцией1. Список препаратов, метаболизируемых с его участием, включает в себя антидепрессанты разных фармакологических групп, антипсихотики, опиоидные анальгетики, тамоксифен, некоторые бета-блокаторы и противоаритмические средства [8]. Распространенными аллелями, соответствующими нормальной ферментной активности, кроме дикого варианта *1, являются *2 и *35, сниженной ферментной активности — *9, *17, *29, *41, отсутствующей — *3, *4, *5, *6, *40; гаплотип CYP2D6*10 занимает промежуточное положение между вариантами сниженной и отсутствующей активности [8]. Также активность фермента может быть повышена вследствие увеличения числа копий аллелей с нормальной ферментной активностью (*1xN, *2xN), что влечет за собой увеличение темпов метаболизма субстратов [8][9].
Объем тестирования генетических вариантов регламентируется международными рекомендациями, разработанными Рабочей группой по фармакогеномике Ассоциации молекулярной патологии (PGxWG AMP) [10–13]. Эти рекомендации предусматривают разделение рекомендованных к тестированию аллелей на минимальный (Tier 1) и расширенный (Tier 2) наборы, где Tier 1 включает варианты с доказанным клиническим воздействием и высокой частотой встречаемости в популяциях, а Tier 2 — менее распространенные аллели.
Другие международные инициативы в области фармакогенетики (Консорциум по внедрению клинической фармакогенетики (Clinical Pharmacogenetics Implementation Consortium, CPIC), Нидерландская рабочая группа по фармакогенетике (Dutch Pharmacogenetics Working Group, DPWG), Европейское агентство лекарственных средств (European Medicines Agency, EMA) не предлагают наборов аллелей, учет которых рекомендован при генотипировании нужных изоферментов цитохрома P450, а вместо этого фокусируются на связи генотип-дозирование и алгоритмах принятия решений в зависимости от генотипа (CPIC, DPWG) либо на аспектах регулирования терминологических стандартов и систематизации биомаркеров в фармакогенетических исследованиях (EMA).
Существующие рекомендации основаны преимущественно на данных западных популяций и не учитывают специфику России, где распределение аллелей может существенно отличаться из-за уникального популяционного состава. В настоящее время отечественные аналоги таких рекомендаций отсутствуют, что создает риск недооценки клинически значимых вариантов у пациентов в РФ.
Цель исследования — определение аллельного полиморфизма цитохромов CYP2C9, CYP2C19, CYP2D6 в популяции жителей РФ с учетом региональных особенностей.
МАТЕРИАЛЫ И МЕТОДЫ
Объект исследования
Исследование проведено на основе популяционной выборки из базы данных популяционных частот (GBD) ФГБУ «ЦСП» ФМБА России2. Объем выборки составил 121 442 человека (57 752 (48,4%) мужчины), средний возраст 50,3 ± 13,9 года; данные представлены в виде М ± SD) из 85 субъектов Российской Федерации. В анализе регионального распределения частот аллельных вариантов объединены участники из г. Москвы и Московской области, г. Санкт-Петербурга и Ленинградской области, г. Севастополя и Республики Крым. Условия набора участников БДПЧ описаны в одной из ранее опубликованных работ [14]. Для сравнительного анализа и формирования регион-специфичных диагностических панелей были отобраны регионы, объем наблюдений в которых составляет 250 человек и более (72 региона РФ).
Выделение, секвенирование ДНК и биоинформатический анализ
Выделение геномной ДНК из образцов цельной крови проводили с помощью набора для выделения высокомолекулярной ДНК с магнитными частицами MagAttract HMW DNA Kit (Qiagen, Германия) с использованием роботизированных станций. Пробоподготовку полногеномных библиотек проводили с применением набора реагентов Illumina DNA Prep согласно рекомендациям производителя (Document # 1000000025416 v10, Illumina, США) и набора индексов IDT-ILMN Nextera DNA UD Indexes Set A и Set B, с дальнейшим контролем качества. Полногеномное секвенирование проводили на приборе Illumina NovaSeq 6000, используя набор реагентов S4 на 300 циклов (Illumina, США) для парно-концевых прочтений 2×150 п.о.
На этапе демультипликации данные секвенирования в формате BCL конвертировались в формат FASTQ программой Illumina bcl2fastq2 v2.20.0.4223. Для контроля качества секвенирования использовалась программа Illumina Sequencing Analysis Viewer v2.4.74, для контроля качества прочтений (формат FASTQ.GZ) — биоинформатический инструмент FastQC v0.11.95. Прочтения выравнивались на референсный геном GRCh38.d1.vd16 с помощью программно-аппаратной платформы Illumina DRAGEN Bio-IT Platform v07.021.510.3.5.77. Контроль качества выравниваний (в формате BAM) выполнялся с помощью DRAGEN, FastQC v0.11.98, samtools v1.13 [15] и mosdepth v0.3.1 [16]. Все образцы успешно прошли контроль качества по ключевым метрикам. Итоговое среднее покрытие по геному для каждого образца составило не менее 30x. Поиск малых генетических вариантов (до 50 п.н.) осуществлялся с помощью программного обеспечения Illumina Strelka2 v2.9.10 [17]. Проверка выборки на наличие в ней дубликатов проводилась с помощью программы Picard CrosscheckFingerprints [18] со встроенным map-файлом. Используемый пайплайн биоинформатической обработки валидирован (F-мера = 99,83%) на эталонном геноме HG001, предоставленном консорциумом Genome In A Bottle (GIAB) (v.3.3.2) [19]. Наличие однонуклеотидных замен определялось по данным vcf-файлов, созданных на этапе поиска малых генетических вариантов. Определение генотипа CYP2C9, CYP2C19, CYP2D6 осуществляли при помощи программного обеспечения PAnno [20].
Анализ данных
Обработка данных и визуализация производились с использованием языка программирования Python (версия 3.9), с использованием библиотек pandas, numpy, matplotlib, seaborn, scipy, и языка программирования R, версия 4.4.1, библиотек dplyr, ggplot2.
Аллельная частота рассчитывалась как количество исследуемых аллелей, разделенное на удвоенное число наблюдений. Частота гетерозиготного и гомозиготного носительства определялась как отношение количества соответствующих генотипов к общему числу наблюдений. Значимыми для потенциального включения в диагностические панели считали варианты с аллельной частотой 1% и более для минимального набора, 0,5% и более — для расширенного набора.
Для сопоставления частот аллельных вариантов, выявленных в исследуемой популяции, с глобальными данными использована стандартизированная система биогеографических групп, разработанная PharmGKB и лабораторией Bustamante [21], включающая 9 групп, выделенных в глобальной аутосомной генетической структуре: африканская/афрокарибская, американская, центрально-южноазиатская, восточноазиатская, европейская, латиноамериканская, ближневосточная, океанийская, субсахарская африканская. Источником данных в этой системе являются проекты «1000 Genomes» и «Human Genome Diversity Project».
В соответствии с аннотацией аллелей, приведенной в PharmGKB [3], для каждого наблюдения в выборке был рассчитан индекс активности (activity score, AS) каждого из изоферментов CYP2C9, CYP2C19 и CYP2D6. Фенотип метаболизма (нормальный, промежуточный, медленный; для CYP2C19 — также быстрый и сверхбыстрый) определяли на основе AS в соответствии с общепринятыми алгоритмами [22–25]. Для удобства расчетов при оценке долей в группах промежуточный и медленный метаболизаторы объединялись и назывались «замедленными», быстрый и сверхбыстрый — «ускоренными».
Для каждого региона, количество наблюдений в котором было равно или превышало 250 человек, рассчитывали долю замедленных метаболизаторов субстратов CYP2C9, CYP2C19 и CYP2D6, а также долю ускоренных метаболизаторов (только для CYP2C19). Оценку долей проводили с построением 95% доверительного интервала (ДИ), рассчитанного методом Вильсона.
Методом интервальной оценки выделялись регионы риска, в которых частота носителей генотипов, ассоциированных с изменением метаболизма исследуемых ферментов, превышала популяционный уровень. Затем с помощью z-критерия с поправкой на множественные сравнения (метод Бенджамини – Хохберга, FDR-контроль на уровне 5%) сравнивались частоты функционально значимых аллелей в регионах риска с общепопуляционными данными.
РЕЗУЛЬТАТЫ
Общая характеристика популяции и аллельные частоты
Распределение аллельных частот и частот носительства в исследованной популяционной выборке для вариантов, встречаемость которых превышает 0,5%, приведено в таблице 1.
Таблица 1. Показатели распространенности аллельных вариантов CYP2C9, CYP2C19, CYP2D6 в общей популяции с аллельной частотой > 0,5%
Аллельный вариант | Частота аллели, % | Частота носительства, % | Частота гетерозиготных носителей в выборке, % | Частота гомозиготных носителей в выборке, % | Рекомендации PGxWG AMP по диагностике |
CYP2C9 | |||||
*1 | 81,31 | 96,38 | 30,13 | 66,24 | Tier 1: *2, *3, *5, *6, *8, *11 Tier 2: *12, *13, *15 |
*2 | 9,59 | 18,2 | 17,23 | 0,97 | |
*3 | 7,76 | 14,82 | 14,11 | 0,7 | |
*29 | 0,98 | 1,91 | 1,88 | 0,04 | |
CYP2C19 | |||||
*1 | 52,99 | 77,63 | 49,11 | 28,52 | Tier 1: *2, *3, *17 Tier 2: *4, *5, *6, *7, *8, *9, *10, *35 |
*17 | 25,55 | 44,19 | 37,2 | 6,99 | |
*2 | 12,81 | 23,73 | 21,96 | 1,77 | |
*38 | 7,5 | 14,36 | 13,69 | 0,67 | |
*3 | 0,58 | 1,14 | 1,11 | 0,03 | |
CYP2D6 | |||||
*1 | 37,86 | 60,06 | 44,35 | 15,7 | Tier 1: *2, *3, *4, *5, *6, *9, *10, *17, *29, *41 Tier 2: *7, *8, *12, *14, *15, *21, *31, *40, *42, *49, *56, *59 |
*2 | 18,13 | 32,06 | 27,84 | 4,22 | |
*4 | 15,29 | 27,48 | 24,42 | 3,06 | |
*35 | 8,98 | 16,64 | 15,32 | 1,32 | |
*41 | 7,37 | 13,87 | 12,99 | 0,88 | |
*10 | 3,68 | 6,5 | 5,64 | 0,86 | |
*33 | 1,91 | 3,71 | 3,6 | 0,11 | |
*9 | 1,51 | 2,94 | 2,86 | 0,08 | |
*3 | 1,12 | 2,19 | 2,14 | 0,06 | |
*6 | 0,9 | 1,76 | 1,73 | 0,04 | |
*39 | 0,85 | 1,58 | 1,45 | 0,13 | |
*59 | 0,68 | 1,32 | 1,28 | 0,04 | |
Таблица составлена авторами по собственным данным
Примечание: строки отсортированы по убыванию частоты аллели, зеленым цветом выделены аллели с встречаемостью менее 1%.
Для гена CYP2C9 перспективными для включения в минимальный набор тестирования вариантами представляются *2 и *3, которые встречаются с частотой более 1%. Аллель CYP2C9*29 может быть потенциально включена в расширенный набор рекомендованной в российской популяции диагностики, так как встречаемость составляет более 0,5%, а носительство — более 1%.
Аллельные варианты CYP2C19, которые преодолевают порог распространенности 1%, кроме «дикого» типа *1, представлены аллелями *17, *2 и *38. При этом CYP2C19*38 соответствует нормальной ферментной активности так же, как и «дикий» тип, поэтому диагностика ее носительства не оправдана. Таким образом, в минимальный набор тестирования вариантов CYP2C19 в РФ разумно включить CYP2C19*2 и CYP2C19*17, а CYP2C19*3, имеющий распространенность менее 1%, внести в расширенный набор диагностики.
Ген CYP2D6 характеризуется значительным аллельным разнообразием, и среди частых для российской популяции вариантов (*2, *3, *4, *9, *10, *33, *35, *41) установленное влияние на активность фермента имеет носительство аллелей *3 (AS = 0), *4 (AS = 0), *9 (AS = 0,5), *10 (AS = 0,5), *41 (AS = 0,5). Данные аллели являются кандидатами для включения в минимальный диагностический набор. Из менее распространенных, но встречающихся с частотой более 0,5% вариантов влиянием на итоговую ферментную активность обладают CYP2D6*6 (AS = 0) и CYP2D6*59 (AS = 0,5).
Исходя из частотного и функционального критериев были сформированы минимальный и расширенный наборы диагностики генотипа изоферментов CYP2C9, CYP2C19 и CYP2D6, актуальные для жителей РФ (рис. 1, табл. 2).

Рисунок подготовлен авторами по собственным данным
Рис. 1. Диагностические панели для генотипирования CYP2C9 и CYP2C19 у жителей РФ в отдельных регионах: А — аллельные варианты CYP2C9; в блоках выделены группы регионов и оптимальная диагностическая панель для них; Б — аллельные варианты CYP2C19; в блоках выделены группы регионов и оптимальная диагностическая панель для них; Уральский ФО — Уральский федеральный округ включает Курганскую, Свердловскую, Тюменскую, Челябинскую области и Ханты-Мансийский и Ямало-Ненецкий автономные округа; ЛО — Ленинградская область; Центральный ФО — Центральный федеральный округ, за исключением Орловской, Тамбовской, Липецкой, Брянской областей, которые не участвовали в анализе ввиду малого количества наблюдений
Таблица 2. Диагностические панели для генотипирования CYP2D6 у жителей отдельных регионов РФ
Регион | Минимальный диагностический набор аллельных вариантов | Расширенный диагностический набор |
Общая популяция | *3, *4, *9, *10, *41 | *6, *59 |
Курганская область | *3, *4, *10, *41 | *6, *9, *59 |
Тульская область Владимирская область Саратовская область | *3, *4, *6, *9, *10, *41, *59 | – |
Республика Карелия Республика Башкортостан | *3, *4, *9, *10, *41, *59 | *6 |
Смоленская область | *3, *4, *9, *10, *41 | *59 |
Республика Мордовия | *3, *4, *6, *9, *10, *41 | – |
Ставропольский край Нижегородская область Белгородская область Калужская область Пензенская область Челябинская область Кемеровская область Архангельская область Ивановская область Тверская область Пермский край Алтайский край Иркутская область Забайкальский край Хабаровский край Ханты-Мансийский АО | *3, *4, *6, *9, *10, *41 | *59 |
Ярославская область Амурская область | *4, *6, *9, *10, *41 | *3 |
Марий Эл | *4, *10, *41 | *3, *6, *9, *32 |
Костромская область | *3, *4, *9, *10, *41, *59 | *6, *32 |
Мурманская область | *3, *4, *10, *41 | *6, *9 |
Дагестан Кабардино-Балкария | *4, *10, *41 | *6, *9, *32 |
Северная Осетия — Алания Адыгея | *4, *10, *41 | *6, *9 |
Республика Ингушетия | *4, *7, *10, *41 | – |
Чувашская Республика | *4, *10, *41 | *6, *9, *32, *59 |
Чеченская Республика | *4, *7, *10, *32, *41 | – |
Тыва | *4, *10, *41 | – |
Якутия Калмыкия | *4, *10, *41 | *3, *9 |
Бурятия | *4, *10, *41 | *3, *6, *9 |
Коми | *3, *4, *6, *9, *10, *41 | – |
Краснодарский край | *4, *6, *10, *41 | *3, *59 |
Республика Крым Самарская область Оренбургская область Удмуртская Республика Сахалинская область | *4, *9, *10, *41 | *3, *6, *59 |
Республика Татарстан Курская область Камчатский край | *4, *9, *10, *41 | *3, *6 |
Новосибирская область Тюменская область | *4, *6, *9, *10, *41 | *3, *59 |
Таблица составлена авторами по собственным данным
Примечание: «–» — отсутствие данных.
Региональные особенности частотного распределения аллелей
Учитывая то, что генетические структуры отдельных регионов России могут сильно различаться, данная общероссийская панель должна быть модифицирована там, где это требуется. Те регионы, в которых аллельное распределение CYP2C9 подразумевало другую оптимальную панель диагностики, выведены на рисунке 1А. Аналогичная информация для CYP2C19 и CYP2D6 представлена на рисунке 1Б и в таблице 2 соответственно.
Большинство отличий характеризовалось перемещением аллели *29 в минимальный набор за счет преодоления ею порога распространенности 1%, причем в республиках Чувашия (6,32%) и Марий Эл (5,61%) наблюдали превышение порога 5%. Вместе с тем наблюдали и некоторые качественные различия: присутствие варианта CYP2C9*11 у жителей Коми, CYP2C9*12 — у жителей Дагестана и Чеченской Республики.
Для жителей значительного количества регионов России, охватывающих практически весь Центральный и Северо-Западный федеральные округа, значительное количество регионов Северо-Кавказского округа и, в меньшей степени, другие макрорегионы, не актуально тестирование аллели CYP2C19*3 даже в рамках расширенной панели, поскольку ее частота не преодолевает порог 0,5%. При этом в республиках Саха, Бурятия, Марий Эл, Башкортостан, Калмыкия, Тыва этот вариант обладает достаточной распространенностью, чтобы рекомендовать тестирование его носительства уже в рамках минимальной диагностической панели. В качественном отношении выделяются Ямало-Ненецкий автономный округ и Забайкальский край, в которых представлена аллель CYP2C19*8 (AS = 0) с частотой 0,51 и 0,58% соответственно.
Ввиду высокого аллельного разнообразия CYP2D6, присутствия в популяционной структуре нескольких аллелей, распространенность которых составляет около 1%, полученное многообразие вариантов диагностических наборов ожидаемо в силу комбинаторных причин. Аллели *4, *10, *41 неизменно присутствовали в минимальном диагностическом наборе во всех исследуемых группах, в силу чего их можно считать наиболее значимыми в отношении генотипирования CYP2D6 для российской популяции. Аллели *3, *6, *9, *59, как правило, присутствуют в одном из наборов. При этом некоторые регионы (республики Северная Осетия, Адыгея, Саха, Тыва, Калмыкия, в меньшей степени Бурятия) характеризовались меньшим генетическим разнообразием в отношении данного фермента, по этой причине представляется оправданным использование в них менее обширных диагностических панелей.
К отличиям качественного характера следует отнести присутствие аллелей *32 (AS = 0,25) и *7 (AS = 0) в некоторых субпопуляциях. CYP2D6*32 встречался в республике Марий Эл в 0,85% случаев, Дагестане (0,75%), Кабардино-Балкарии (0,79%), Чувашии (0,67%), Чечне (1,43%) и Костромской области (0,52%). Значимое присутствие в аллельной структуре для CYP2D6*7 было выявлено в Ингушетии (1,39%) и Чечне (1,64%).
В ряде исследованных нами выборок также были представлены редкие аллели*74 и *117 с неизвестной функцией, по причине чего они не были внесены в диагностические наборы. CYP2D6*74 встречался в Хабаровском крае (0,53%), Пензенской (0,6%) и Калужской (0,52%) областях, Забайкальском (0,8%) и Камчатском (0,69%) краях. В свою очередь, носительство CYP2D6*117 с частотой более 0,5% было зарегистрировано в некоторых северных регионах (Архангельская область — 0,58%, Вологодская область — 0,56%, Республика Карелия — 0,87%, Мурманская область — 0,53%), а также в Тюменской области (0,58%) и Пермском крае (0,68%).
Сопоставление с мировыми данными
Сравнение частот аллельных вариантов цитохромов CYP2C9, CYP2C19 и CYP2D6, выявленных в исследуемой популяции, с глобальными данными (рис. 2) демонстрировало сходство частотного распределения аллелей данных ферментов в популяционной выборке РФ с таковым в общеевропейской популяции. Аллель CYP2C19*38 не учитывали в данном анализе, поскольку в более ранних номенклатурах она рассматривалась как субаллель дикого типа CYP2C19*1.001 [26] и по этой причине в используемых нами ресурсах о мировом аллельном распределении приравнивается к CYP2C19*1.

Рисунок подготовлен авторами по собственным данным
Рис. 2. Распределение аллелей изоферментов CYP2C9 (А), CYP2C19 (Б), CYP2D6 (В), встречающихся в российской популяции с частотой > 1%, в основных биогеографических группах: частоты аллелей (ось Y) представлены в абсолютных величинах; по оси Х представлены популяции: RUS — российская (выборка настоящего исследования); EUR — Европы и жителей США европейского происхождения; EAS — восточноазиатская (Китай, Япония, Корея, частично Юго-Восточная Азия); NEA — ближневосточная (Ближний Восток, Кавказ, Северная Африка); SAS — южно- и центральноазиатская (Пакистан, Индия, Бангладеш); LAT — латиноамериканская, группы со смешанным индейским, европейским и африканским происхождением; AAC — афрокарибская; SSA — африканская к югу от Сахары; AME — коренные народы Северной и Южной Америки, OCE — коренное население Австралии, Океании и Новой Гвинеи
Присутствие в популяционной выборке РФ аллели CYP2C9*29 (около 1%), которая мало представлена в популяции европейцев (0,03%) и отсутствует в остальных биогеографических группах, за исключением восточноазиатской, где ее распространенность также невысока (0,22%), является наиболее заметным отличием российской выборки. Аллель CYP2D6*10 в популяции РФ встречалась достоверно чаще, чем в европейской (3,7% против 1,57%, р = 0,000), что, вероятно, обусловлено ближневосточными (6,77%) и восточноазиатскими (42,84%) влияниями.
Типы метаболизма субстратов CYP2C9, CYP2C19, CYP2D6: общепопуляционная оценка и выделение регионов риска
В общей популяции генотип CYP2C9, соответствующий нормальному метаболизму его субстратов (AS = 2), встречался с частотой 66,34%, промежуточному метаболизму (1 ≤ AS < 2) — 31,35%, медленному (AS < 1) — 2,31%. Таким образом, суммарно доля лиц, имеющих сниженную ферментную активность CYP2C9, составила 33,66%, то есть около ⅓ населения. Региональное распределение доли лиц, имеющих сниженную ферментную активность CYP2C9, приведено на рисунке 4.
Исходя из полученных интервальных оценок могут быть выделены шесть субъектов, в которых частота носительства генотипа, ассоциированного со сниженным метаболизмом субстратов CYP2C9, достоверно выше общепопуляционной. Такими регионами риска являются Чеченская Республика, Дагестан, Ингушетия, Кабардино-Балкария, Северная Осетия, Чувашия, Марий Эл, Удмуртская Республика, Татарстан. Напротив, благополучными с этой точки зрения являются республики Бурятия, Калмыкия, Тыва и Якутия. Для уточнения картины аллельного распределения в регионах риска проведено сравнение частот встречаемости вариантов CYP2C9 с общепопуляционными оценками (рис. 3Б, 3В).

Рисунок подготовлен авторами по собственным данным
Рис. 3. Популяционные характеристики аллельного полиморфизма CYP2C9: А — региональное распределение доли носителей генотипов CYP2C9, соответствующих замедленному метаболизму субстратов фермента (представлены регионы с долей, отличающейся от популяционной); Б — популяционное аллельное распределение CYP2C9; В — аллельное распределение CYP2C9 в регионах с увеличенной частотой носительства генотипов медленного/промежуточного метаболизма в сравнении с популяционным
Примечание: красная пунктирная линия отражает популяционную оценку; КБР — Кабардино-Балкарская Республика; РД — Республика Дагестан; РИ — Республика Ингушетия; РМЭ — Республика Марий Эл; РСО — Республика Северная Осетия — Алания; РТат — Республика Татарстан; УР — Удмуртская Республика; ЧечР — Чеченская Республика; ЧувР — Чувашская Республика «*» — частоты, статистически значимо отличающиеся от популяционных (p-adj < 0,05).
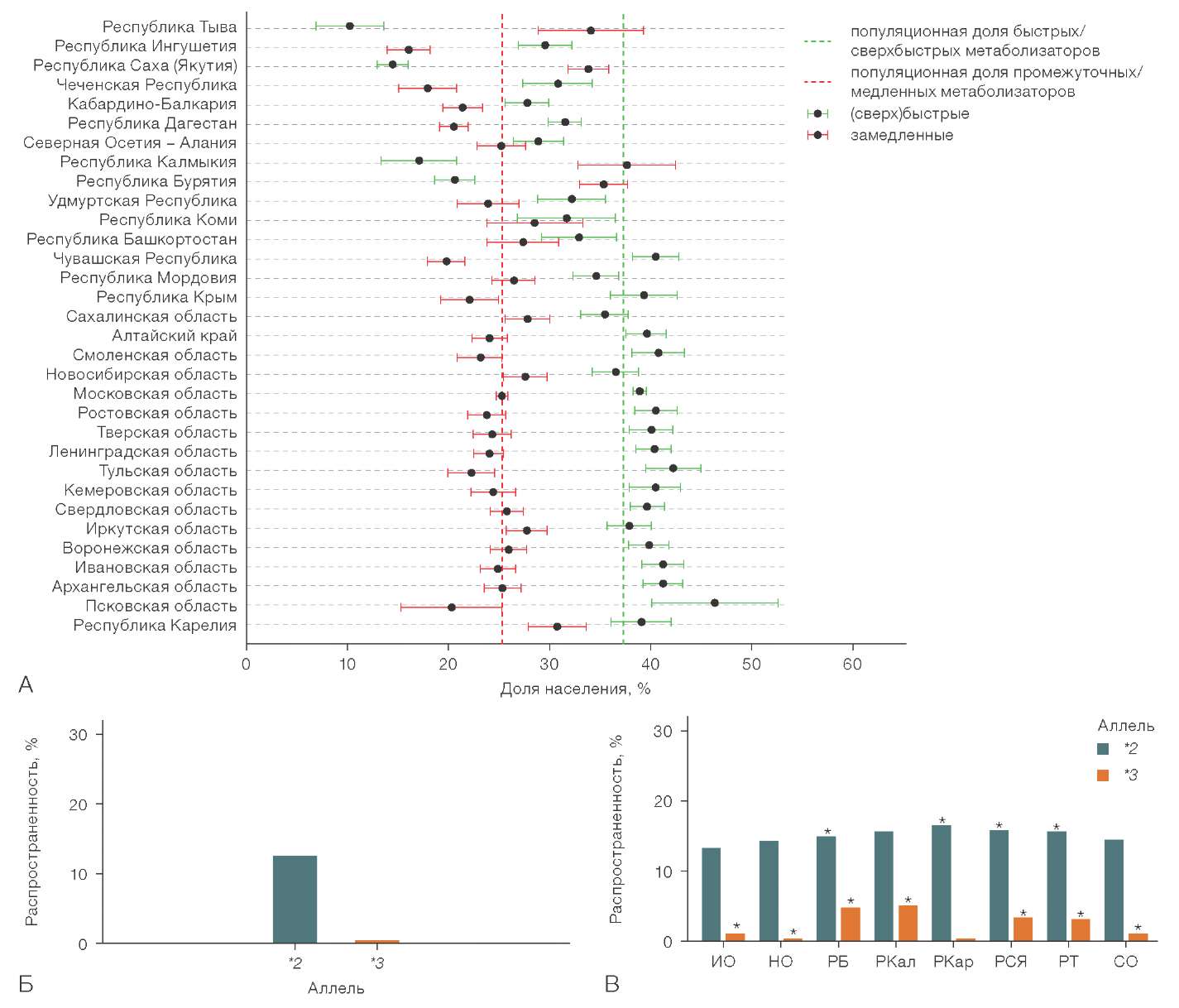
Рисунок подготовлен авторами по собственным данным
Риc. 4. Популяционные характеристики аллельного полиморфизма CYP2C19: А — региональное распределение метаболических фенотипов CYP2C19 (представлены регионы с долей, отличающейся от популяционной); Б – популяционное аллельное распределение CYP2C19; В — аллельное распределение CYP2C19 в регионах с увеличенной частотой носительства генотипов медленного/промежуточного метаболизма в сравнении с популяционным
Примечание: РТ — Республика Тыва; РСЯ — Республика Саха (Якутия); РКал — Республика Калмыкия; РБ — Республика Бурятия; РКар — Республика Карелия; СО — Сахалинская область; НО — Новосибирская область; ИО — Иркутская область «*» — частоты, статистически значимо отличающиеся от популяционных (p-adj < 0,05).
Полученные результаты продемонстрировали неоднородность выделенных нами регионов риска по внесенному вкладу тех или иных аллельных вариантов в повышение вероятности носительства сниженного метаболизма субстратов CYP2C9. Так, данный риск реализовался за счет увеличения частоты носительства аллели CYP2C9*3 в республиках Чечня (18,89%, p-adj = 9,4×10-27), Кабардино-Балкария (12,68%, p-adj = 3,8×10-13), Дагестан (17,69%, p-adj = 1,7×10-89), Ингушетия (18,28%, p-adj = 3,1×10-40),Северная Осетия (11,04%, p-adj = 9,3×10-5), в дополнение к этому в Чечне и Дагестане несколько выше представленность аллели CYP2C9*12 (0,71%, p-adj = 2,1×10-19 и 0,04%, p-adj = 8,3×10-22 соответственно). Вместе с тем аллель CYP2C9*29 относительно высоко распространена в республиках Марий Эл (5,61%, p-adj = 1,1×10-43), Чувашия (6,32%, p-adj = 3,3×10-104), Татарстан (2,15%, p-adj = 2,5×10-5), Удмуртия (2,17%, p-adj = 0,009), однако распространенность аллелей *2 и *3 в этих регионах сопоставима с общепопуляционной.
В исследованной нами выборке большинство людей имело нормальный (37,26%) или быстрый (30,38%) тип метаболизма субстратов CYP2C19. Доля носителей генотипов промежуточного метаболизма составляла 23,26%, сверхбыстрого (*17/*17) — 6,99%, медленного — 2,11%. Доли носителей генотипов замедленного и ускоренного метаболизма составляли 25,37 и 37,37% соответственно. Региональные различия долей ускоренных и замедленных метаболизаторов представлены на рисунке 4А.
Республики Тыва, Якутия, Калмыкия и Бурятия характеризовались существенным снижением доли лиц с фенотипом ускоренного метаболизма и одновременным значительным увеличением процента замедленных метаболизаторов, последнее также справедливо в меньшей степени выраженности для Сахалинской, Иркутской и Новосибирской областей, а также Республики Карелия. Такие регионы, как Ингушетия, Чечня, Кабардино-Балкария, Дагестан, имели более низкие по сравнению с популяционными доли как ускоренных, так и замедленных метаболизаторов субстратов фермента CYP2C19. Увеличение представленности быстрого/сверхбыстрого фенотипа метаболизма наблюдали у жителей Чувашии, Алтайского края, Смоленской, Московской, Ростовской, Тверской, Ленинградской, Тульской, Кемеровской, Воронежской, Ивановской, Архангельской, Псковской областей.
Изменение доли носителей быстрого или сверхбыстрого метаболизма может быть реализовано только за счет изменения распространенности аллели *17, так как только она ассоциирована с увеличением ферментной активности CYP2C19. Для регионов с увеличенным носительством фенотипа замедленного метаболизма (Тыва, Якутия, Калмыкия, Бурятия, Карелия, Сахалинская, Новосибирская, Иркутская области) уточнялся характер аллельного распределения по сравнению с популяционным (рис. 4Б, 4В).
Полученные результаты распределения аллельных вариантов в регионах риска замедленного метаболизма субстратов CYP2C19 показывают, что данный риск реализуется не за счет присутствия редких аллелей в этих географических группах, а в силу большей представленности медленных аллелей, которые также распространены в общей популяции CYP2C19*3 и в меньшей степени CYP2C19*2.
Исследованная нами популяционная выборка характеризовалась нормальным метаболизмом субстратов CYP2D6 в 91,72% случаев. Промежуточный тип метаболизма встречался в 4,32% наблюдений, сниженный — 3,97%. Доля замедленного метаболизма для популяции в целом составляла 8,29%; соответствующие данные представлены на рисунке 5А.
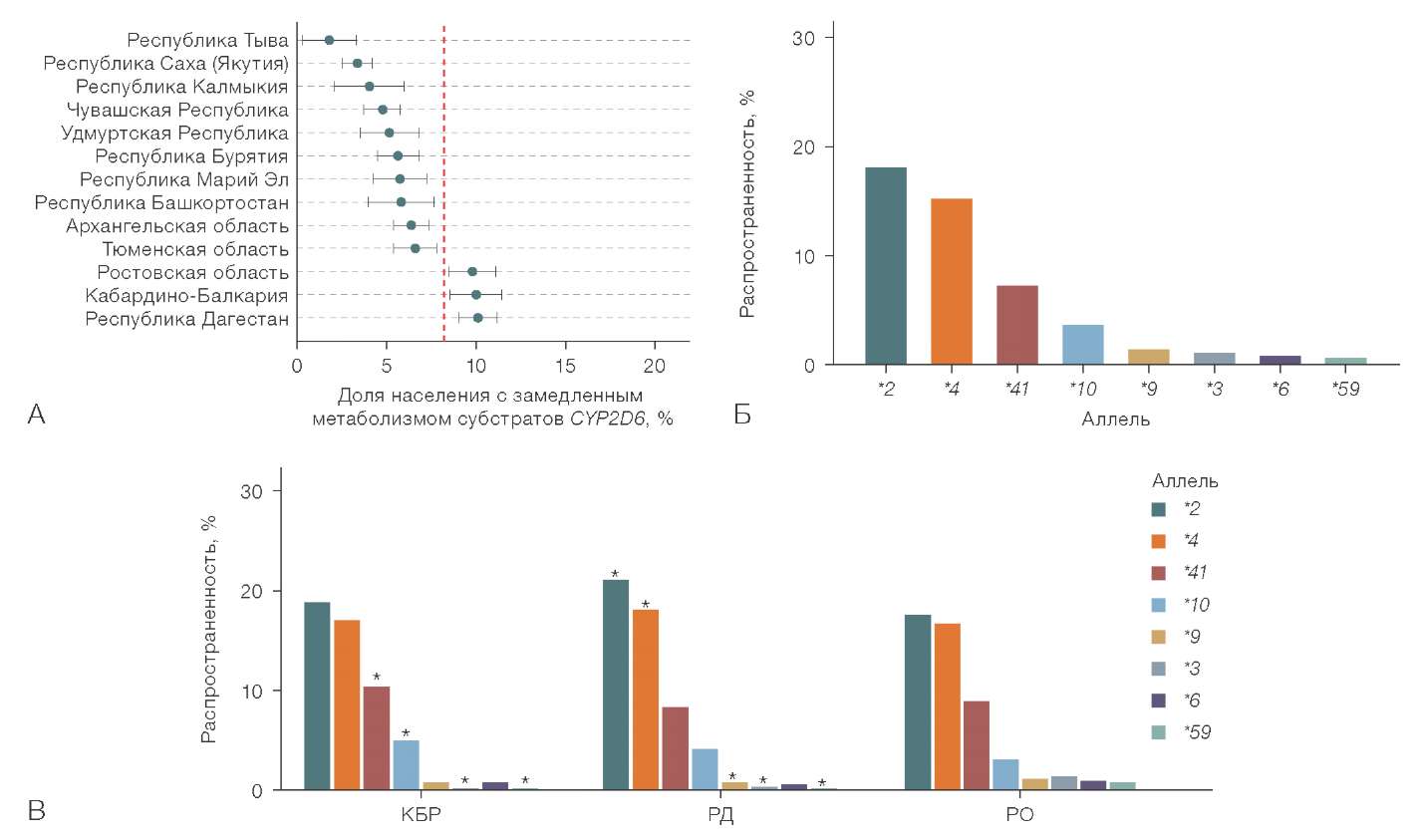
Рисунок подготовлен авторами по собственным данным
Рис. 5. Аллельное распределение для CYP2D6 в Ростовской области, Дагестане, Кабардино-Балкарии: А — региональное распределение доли носителей генотипов CYP2D6, соответствующих замедленному метаболизму субстратов фермента (представлены регионы с долей, отличающейся от популяционной); Б — популяционное аллельное распределение CYP2D6; В — аллельное распределение CYP2D6 в регионах с увеличенной частотой носительства генотипов медленного/промежуточного метаболизма в сравнении с популяционным; РО — Ростовская область; КБР — Кабардино-Балкарская Республика; РД — Республика Дагестан
Примечание: «*» — частоты, статистически значимо отличающиеся от популяционных (p-adj < 0,05).
Низкий риск носительства генотипа, соответствующего замедленному метаболизму субстратов фермента, имели жители Тывы, Якутии, Калмыкии, Чувашии, Удмуртской Республики, Бурятии, Марий Эл, Башкортостана, Архангельской области. Несколько большую долю носителей промежуточного/медленного метаболизма регистрировали в Ростовской области (9,84%), Дагестане (10,17%) и Кабардино-Балкарии (10,05%). Аллельное распределение для CYP2D6 в этих регионах представлено на рисунках 5Б, 5В.
При сравнении встречаемости отдельных аллелей в регионах риска с общепопуляционными оценками было выявлено, что в Кабардино-Балкарской Республике выше встречаемость CYP2D6*41 (10,46%, p-adj = 1,3×10-5) и CYP2D6*10 (4,92%, p-adj = 0,022), в Республике Дагестан — аллелей CYP2D6*2 (20,96%, p-adj = 1,5×10-4) и CYP2D6*4 (17,98%, p-adj = 1,5×10-4). В Ростовской области после введения поправки на множественные сравнения различий встречаемости основных аллелей не выявлено.
ОБСУЖДЕНИЕ
Результаты проведенного исследования, полученные на крупной и репрезентативной популяционной выборке, вносят вклад в понимание аллельного полиморфизма CYP2C9, CYP2C19, CYP2D6 в российской популяции и создают предпосылки для спецификации объема фармакогенетического тестирования на региональном уровне. Широкое внедрение такого тестирования, являющегося неотъемлемой частью персонализированной медицины, невозможно без создания доступных инструментов диагностики, которые, в свою очередь, ограничиваются некоторым заранее определенным набором тестируемых вариантов. Наши результаты показывают, что наборы, сформулированные в рекомендациях AMP, не оптимальны для использования в российской клинической практике.
Предлагаемый AMP минимальный набор тестируемых аллелей для CYP2C9 охватывает гаплотипы *2, *3, *5, *6, *8, *11, расширенный — *12, *13, *15 [11], при этом из них в российской популяции все варианты, кроме *2 и *3, имеют частоту встречаемости менее 0,5%, что делает тестирование их носительства нерациональным. Рекомендации AMP ориентированы в первую очередь на жителей Соединенных Штатов Америки и Европы, и включение большей части этих аллелей в данные рекомендации, вероятно, связано с относительно высокой их распространенностью у лиц африканского происхождения [6]. В свою очередь, CYP2C9*29, встречающийся приблизительно у 2% населения России и сопровождающийся снижением ферментной активности CYP2C9 (AS = 0,5), не включен даже в расширенный набор рекомендаций AMP.
В минимальный набор генотипирования CYP2C19, предлагаемый AMP, включены гаплотипы *2, *3, *17 [12]; при этом, согласно нашим данным, CYP2C19*3 скорее требует включения в минимальную диагностическую панель лишь в некоторых регионах, но не в популяции в целом, так как распространенность составляет менее 1%. В силу отсутствия функциональной роли этот вариант не был нами включен в потенциальные диагностические панели для CYP2C19. Предлагаемые AMP аллели для расширенной диагностики (*4, *5, *6, *7, *8, *9, *10, *35) не преодолевают порога распространенности 0,5% в российской популяции, поэтому целесообразность их включения в расширенные отечественные диагностические наборы представляется сомнительной.
Для рекомендаций в отношении генотипирования CYP2D6 областью пересечения является набор аллелей *2, *3, *4, *9, *10, *41. Гаплотипы *5, *6, *17, *29 не актуальны для российской популяции, однако входят в минимальный набор AMP [10], вероятно, также ввиду высокой встречаемости в африканской и латиноамериканской популяциях. Потенциальными кандидатами на включение в расширенный набор диагностической панели для российской популяции являются аллели *6 (AS = 0), *59 (AS = 0,5), так как они имеют не исключительно редкую встречаемость и характеризуются влиянием на ферментную активность. Из них в расширенном списке, предлагаемом AMP, присутствует только аллель CYP2D6*59 и в то же время фигурирует свыше десяти других аллелей, неактуальных для жителей России.
Региональные различия аллельной структуры отражают генетическую неоднородность населения РФ. В популяции жителей Республики Коми вариант CYP2C9*11 (AS = 0,5) соответствовал критерию включения в расширенный диагностический набор (распространенность 0,71%). Указанный вариант, согласно мировым данным, встречается только у выходцев из Африки к югу от Сахары [21] и включен в минимальный набор АМР. Сходная ситуация наблюдается для варианта CYP2C9*12 (AS = 0,5), встречающегося у жителей Дагестана (0,75%) и Чеченской Республики (0,72%) и не встречающегося в мировых популяциях, за исключением смешанной ближневосточной с крайне низкой (менее 0,1%) распространенностью [21].
Из крайне редко встречающихся в глобальных популяциях гаплотипов CYP2C19 нами был обнаружен вариант *8 (AS = 0) у жителей Ямало-Ненецкого автономного округа (0,51%) и Забайкальского края (0,58%), при этом аллель совсем не встречается у лиц восточноазиатского происхождения, что можно было бы ожидать, принимая во внимание географию данных регионов, а его учет не рекомендован AMP даже в рамках расширенного набора. Гаплотипы CYP2D6*32, CYP2D6*74, CYP2D6*117, представленные в отдельных регионах РФ, не входят в диагностические наборы AMP. CYP2D6*32 характеризуется сниженной ферментной активностью (AS = 0,25) и встречается исключительно редко только в общеевропейской (0,3%), центрально-южноазиатской (0,2%) и южноафриканской (0,04%) популяциях9, при этом в Чеченской Республике его распространенность превышает 1%, в Марий Эл, Чувашии, Дагестане и Кабардино-Балкарии составляет 0,5–1%.
Для CYP2D6*74 и CYP2D6*117 функциональная роль не определена, однако, согласно рекомендациям CPIC, носители этих вариантов считаются промежуточными метаболизаторами [22][27]. Мы не включали их в рекомендуемые для диагностики панели ввиду недостаточно строгих свидетельств в пользу их функционального значения, однако по мере накопления данных позиция в отношении необходимости их учета может быть пересмотрена. CYP2D6*74, встречающийся с частотой 0,5–0,6% в Хабаровском, Забайкальском и Камчатском краях, Пензенской, Калужской областях, не встречается ни в одной биогеографической группе, за исключением жителей Африки, а CYP2D6*117 встречается исключительно у европейцев с частотой менее 1%10.
Наиболее крупные российские биотехнологические компании, изготавливающие реагентные компоненты для полимеразной цепной реакции, имеют в своей продуктовой линейке праймеры для определения носительства CYP2C9*2 и CYP2C9*3. Таким образом, учет актуальных для российской популяции аллелей CYP2C9*29 и, в меньшей степени, CYP2C9*12 возможен только в рамках полногеномного секвенирования, но не рутинными средствами диагностики. Для CYP2C19 доступный набор тестирования (CYP2C19*2, CYP2C19*3, CYP2C19*17) охватывает необходимый для большинства регионов набор вариантов, за исключением Ямало-Ненецкого автономного округа и Забайкальского края, где относительную актуальность представляет тестирование носительства CYP2C19*8 в рамках расширенной диагностики. Учитывая высокую вариабельность гена CYP2D6, объем диагностики также достаточно обширен и включает в себя установление носительства аллелей *3, *4, *10, *41, *6, *9, кроме того, частные лаборатории осуществляют определение делеции (*5) и дупликации гена. В оптимальный набор для тестирования населения РФ также следовало бы включить аллель *59, а в отдельных регионах — *32 и *7.
Важным ограничением нашего исследования является анализ только однонуклеотидных полиморфизмов и гаплотипов, предсказываемых на их основе. Структурные варианты, такие как крупные делеции (например, CYP2D6*5) или вариации числа копий генов (например, CYP2D6*1xN), не учитывались из-за невозможности точного определения копийности гена либо других крупных структурных вариаций по данным короткоридового полногеномного секвенирования со средним покрытием 30–40х. Это могло привести к недооценке частот некоторых клинически значимых аллелей, где структурные варианты вносят существенный вклад в фенотип метаболизма. Согласно литературным данным, CYP2D6*1xN распространен в восточноазиатской популяции [6], по этой причине можно было бы ожидать схожую картину в восточных регионах России.
Помимо этого, необходимо отметить, что предложенные региональные панели служат важной основой для персонализации фармакотерапии, однако их внедрение в клиническую практику требует предварительного клинико-экономического обоснования. Важно оценить баланс между затратами на генетическое тестирование и потенциальным ущербом от неучета функционально значимых вариантов. Для препаратов с узким терапевтическим индексом предварительное генотипирование может быть экономически оправданным при благоприятном профиле переносимости и отсутствии серьезных угроз, при неэффективности — избыточен. Таким образом, при разработке клинических рекомендаций должны быть учтены не только популяционно-генетические данные, но и тяжесть и риски предотвращаемых нежелательных реакций, стоимостные параметры и клинические исходы для конкретных лекарственных средств.
ЗАКЛЮЧЕНИЕ
Российская популяция в целом характеризуется сходством с общеевропейской в отношении аллельного полиморфизма CYP2C9, CYP2C19, CYP2D6, однако имеет отличительные черты как на общепопуляционном уровне, так и на уровне отдельных регионов, демонстрируя популяционную гетерогенность. Это подчеркивает важность не только разработки отечественных диагностических панелей, но и дифференцированного подхода к фармакогенетическому тестированию в разных биогеографических группах внутри страны. Установлена представленность исключительно редких по общемировым меркам аллелей CYP2C9*29, CYP2C9*11, CYP2C9*12, CYP2C19*8, CYP2D6*32, CYP2D6*7, CYP2D6*74, CYP2D6*117 в популяционной структуре либо в отдельных биогеографических группах Российской Федерации. Внедрение предложенных диагностических панелей в клиническую практику должно сопровождаться клинико-экономическим обоснованием для каждого препарата, чья эффективность или безопасность существенно зависят от генотипа CYP2C9, CYP2C19 и CYP2D6.
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Наибольший вклад распределен следующим образом: В.С. Юдин — концептуализация; Е.Д. Спектор — методология, создание рукописи; А.А. Мамчур — визуализация; М.В. Иванов — формальный анализ; С.И. Митрофанов — программное обеспечение; Л.П. Кузьмина — ресурсы; И.В. Бухтияров — проведение исследования; А.А. Кескинов — администрирование проекта; С.М. Юдин — руководство исследованием; Д.А. Каштанова — редактирование рукописи.
1. PharmGKB. URL: https://www.pharmgkb.org
2. База данных популяционных частот генетических вариантов населения Российской Федерации. ФМБА России. Версия приложения 1.1.3 от 17.03.2025. Версия базы 59.1 от 03.10.2024.
3. bcl2fastq and bcl2fastq2 Conversion Software Downloads. URL: https://emea.support.illumina.com/sequencing/sequencing_software/bcl2fastq-conversion-software/downloads.html
4. Sequencing Analysis Viewer Support. URL: https://support.illumina.com/sequencing/sequencing_software/sequencing_analysis_viewer_sav.html
5. Babraham Bioinformatics — FastQC A Quality Control tool for High Throughput Sequence Data. URL: https://www.bioinformatics.babraham.ac.uk/projects/fastqc/
6. GDC Reference Files | NCI Genomic Data Commons. URL: https://gdc.cancer.gov/about-data/gdc-data-processing/gdc-reference-files
7. DRAGEN secondary analysis | Software for NGS data analysis. URL: https://www.illumina.com/products/by-type/informatics-products/dragen-secondary-analysis.html
8. Babraham Bioinformatics — FastQC A Quality Control tool for High Throughput Sequence Data. URL: https://www.bioinformatics.babraham.ac.uk/projects/fastqc/
9. PharmGKB. URL: https://www.pharmgkb.org
10. Там же.
Список литературы
1. Dawes M, Aloise MN, Ang S, Cullis P, Dawes D, Fraser R, et al. Introducing pharmacogenetic testing with clinical decision support into primary care: a feasibility study. CMAJ Open. 2016;4(3):E528–34. https://doi.org/10.9778/cmajo.20150070
2. Baltzer Houlind M, Hansen L, Iversen E, Rasmussen HB, Larsen JB, Jorgensen S, et al. Pharmacogenetic testing of CYP2D6, CYP2C19 and CYP2C9 in Denmark: Agreement between publicly funded genotyping tests and the subsequent phenotype classification. Basic and Clinical Pharmacology and Toxicology. 2024;134(5):756–63. https://doi.org/10.1111/bcpt.13990
3. Barbarino JM, Whirl-Carillo M, Altman RB, Klein TE. PharmGKB: A worldwide resource for pharmacogenomic information. WIREs. 2018;10(4):e1417. https://doi.org/10.1002/wsbm.1417
4. Zhang H-F, Wang H-H, Gao N, Wei JY, Tian X, Zhao Y, et al. Physiological Content and Intrinsic Activities of 10 Cytochrome P450 Isoforms in Human Normal Liver Microsomes. Journal of Pharmacology and Experimental Therapeutics. 2016;358(1):83–93. https://doi.org/10.1124/jpet.116.233635
5. Daly AK, Rettie AE, Fowler DM, Miners JO. Pharmacogenomics of CYP2C9: Functional and Clinical Considerations. Journal of Personalized Medicine. 2017;8(1):1. https://doi.org/10.3390/jpm8010001
6. Zhou Y, Ingelman-Sundberg M, Lauschke VM. Worldwide Distribution of Cytochrome P450 Alleles: A Meta-analysis of Population-scale Sequencing Projects. Clinical Pharmacology and Therapeutics. 2017;102(4):688–700. https://doi.org/10.1002/cpt.690
7. Shubbar Q, Alchakee A, Issa KW, Adi AJ, Shorbagi AI, Saber-Ayad M. From genes to drugs: CYP2C19 and pharmacogenetics in clinical practice. Frontiers in Pharmacology. 2024;15:1326776. https://doi.org/10.3389/fphar.2024.1326776
8. Pratt VM, Scott SA, Pirmohamed M, Esquivel B, Kattman BL, Malheiro AJ, ed. Medical Genetics Summaries. Bethesda (MD): National Center for Biotechnology Information (US);2012.
9. Gong L, Klein CJ, Caudle KE, Moyer AM, Scott SA, Whirl-Carillo M, et al. Integrating Pharmacogenomics into the Broader Construct of Genomic Medicine: Efforts by the ClinGen Pharmacogenomics Working Group (PGxWG). Clinical Chemistry. 2025;71(1):36–44. https://doi.org/10.1093/clinchem/hvae181
10. Pratt VM, Cavallari LH, Del Tredici AL, Hachad H, Ji Y, Moyer AM, et al. Recommendations for Clinical CYP2C9 Genotyping Allele Selection: A Joint Recommendation of the Association for Molecular Pathology and College of American Pathologists. Journal of Molecular Diagnostics. 2019;21(5):746–55. https://doi.org/10.1016/j.jmoldx.2019.04.003
11. Pratt VM, Del Tredici AL, Hachad H, Ji Y, Kalman LV, Scott SA, et al. Recommendations for Clinical CYP2C19 Genotyping Allele Selection: A Report of the Association for Molecular Pathology. Journal of Molecular Diagnostics. 2018;20(3):269–76. https://doi.org/10.1016/j.jmoldx.2018.01.011
12. Pratt VM, Cavallari LH, Fulmer ML, Gaedigk A, Hachad H, Ji Y, et al. CYP3A4 and CYP3A5 Genotyping Recommendations: A Joint Consensus Recommendation of the Association for Molecular Pathology, Clinical Pharmacogenetics Implementation Consortium, College of American Pathologists, Dutch Pharmacogenetics Working Group of the Royal Dutch Pharmacists Association, European Society for Pharmacogenomics and Personalized Therapy, and Pharmacogenomics Knowledgebase. Journal of Molecular Diagnostics. 2023;25(9):619–29. https://doi.org/10.1016/j.jmoldx.2023.06.008
13. Gusakova M, Dzhumaniazova I, Zelenova E, Kashtanova D, Ivanov M, Mamchur A, et al. Prevalence of the cancer-associated germline variants in Russian adults and long-living individuals: using the ACMG recommendations and computational interpreters for pathogenicity assessment. Frontiers in Oncology. 2024;14:1420176. https://doi.org/10.3389/fonc.2024.1420176
14. Li H, Handsaker B, Wysoker A, Fennel T, Ruan J, Homer N, et al. The Sequence Alignment/Map format and SAMtools. Bioinformatics. 2009;25(16):2078–9. https://doi.org/10.1093/bioinformatics/btp352
15. Pedersen BS, Quinlan AR. Mosdepth: quick coverage calculation for genomes and exomes. Bioinformatics. 2018;34(5):867–8. https://doi.org/10.1093/bioinformatics/btx699
16. Kim S, Scheffler K, Halpern AL, Bekritsky MA, Noh E, Kallberg M, et al. Strelka2: fast and accurate calling of germline and somatic variants. Nature Methods. 2018;15(8):591–4. https://doi.org/10.1038/s41592-018-0051-x
17. Najafov J, Najafov A. CrossCheck: an open-source web tool for high-throughput screen data analysis. Scientific Reports. 2017;7(1):5855. https://doi.org/10.1038/s41598-017-05960-3
18. Krusche P, Trigg L, Boutros PC, Mason CE, De La Vega FM, Moore BL, et al. Best practices for benchmarking germline small-variant calls in human genomes. Nature Biotechnology. 2019;37(5):555–60. https://doi.org/10.1038/s41587-019-0054-x
19. Liu Y, Lin Z, Chen Q, Chen Q, Sang L, Wang Y, et al. PAnno: A pharmacogenomics annotation tool for clinical genomic testing. Frontiers in Pharmacology. 2023;14:1008330. https://doi.org/10.3389/fphar.2023.1008330
20. Huddart R, Fohner AE, Whirl-Carillo M, Wojcik GL, Gignoux CR, Popejoy AB, et al. Standardized Biogeographic Grouping System for Annotating Populations in Pharmacogenetic Research. Clinical Pharmacology and Therapeutics. 2019;105(5):1256–62. https://doi.org/10.1002/cpt.1322
21. Karnes JH, Rettie AE, Somogyi AA, Huddart R, Fohner AE, Formea CM, et al. Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline for CYP2C9 and HLA-B Genotypes and Phenytoin Dosing: 2020 Update. Clinical Pharmacology and Therapeutics. 2021;109(2):302–9. https://doi.org/10.1002/cpt.2008
22. Bousman CA, Stevenson JM, Ramsey LB, Sangkuhl K, Hicks JK, Strawn JR, et al. Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline for CYP2D6, CYP2C19, CYP2B6, SLC6A4, and HTR2A Genotypes and Serotonin Reuptake Inhibitor Antidepressants. Clinical Pharmacology and Therapeutics. 2023;114(1):51–68. https://doi.org/10.1002/cpt.2903
23. Hicks JK, Sangkuhl K, Swen JJ, Ellingrod VL, Muller DJ, Shimoda K, et al. Clinical pharmacogenetics implementation consortium guideline (CPIC) for CYP2D6 and CYP2C19 genotypes and dosing of tricyclic antidepressants: 2016 update. Clinical Pharmacology and Therapeutics. 2017;102(1):37–44. https://doi.org/10.1002/cpt.597
24. Lee CR, Luzum JA, Sangkuhl K, Gammal RS, Sabatine MS, Stein CM, et al. Clinical Pharmacogenetics Implementation Consortium Guideline for CYP2C19 Genotype and Clopidogrel Therapy: 2022 Update. Clinical Pharmacology and Therapeutics. 2022;112(5):959–67. https://doi.org/10.1002/cpt.2526
25. Botton MR, Whirl-Carillo M, Del Tredici AL, Sangkuhl K, Cavallari LH, Agundez JAG, et al. PharmVar GeneFocus: CYP2C19. Clinical Pharmacology and Therapeutics. 2021;109(2):352–66. https://doi.org/10.1002/cpt.1973
26. Bousman CA, Stevenson JM, Ramsey LB, Sangkuhl K, Hicks JK, Strawn JR, et al. Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline for CYP2D6, CYP2C19, CYP2B6, SLC6A4, and HTR2A Genotypes and Serotonin Reuptake Inhibitor Antidepressants. Clinical Pharmacology and Therapeutics. 2023;114(1):51–68. https://doi.org/10.1002/cpt.2903
Об авторах
В. С. ЮдинРоссия
Юдин Владимир Сергеевич, канд. биол. наук
Москва
Е. Д. Спектор
Россия
Спектор Екатерина Дмитриевна, канд. мед. наук
Москва
А. А. Мамчур
Россия
Мамчур Александра Александровна
Москва
М. В. Иванов
Россия
Иванов Михаил Вячеславович
Москва
С. И. Митрофанов
Россия
Митрофанов Сергей Игоревич, канд. биол. наук
Москва
Л. П. Кузьмина
Россия
Кузьмина Людмила Павловна, д-р мед. наук, профессор
Москва
И. В. Бухтияров
Россия
Бухтияров Игорь Валентинович, д-р мед. наук, профессор
Москва
А. А. Кескинов
Россия
Кескинов Антон Артурович, канд. мед. наук
Москва
С. М. Юдин
Россия
Юдин Сергей Михайлович, д-р мед. наук, профессор
Москва
Д. А. Каштанова
Россия
Каштанова Дарья Андреевна, канд. мед. наук
Москва
Рецензия
Для цитирования:
Юдин В.С., Спектор Е.Д., Мамчур А.А., Иванов М.В., Митрофанов С.И., Кузьмина Л.П., Бухтияров И.В., Кескинов А.А., Юдин С.М., Каштанова Д.А. Аллельные варианты цитохромов CYP2C9, CYP2C19, CYP2D6 у жителей России: распространенность и региональное распределение. Экстремальная биомедицина. 2026;28(1):37-50. https://doi.org/10.47183/mes.2025-371
For citation:
Yudin V.S., Spektor E.D., Mamchur A.A., Ivanov M.V., Mitrofanov S.I., Kuzmina L.P., Bukhtiyarov I.V., Keskinov A.A., Yudin S.M., Kashtanova D.A. Allelic variants of CYP2C9, CYP2C19, CYP2D6 cytochromes in the Russian population: Prevalence and regional distribution. Extreme Medicine. 2026;28(1):37-50. https://doi.org/10.47183/mes.2025-371
JATS XML
















