Перейти к:
Современный подход в микрохирургическом устранении дефектов языка с применением компьютерного цифрового планирования
https://doi.org/10.47183/mes.2024-26-3-98-105
Аннотация
Введение. Принцип лечения злокачественных новообразований слизистой оболочки ротовой полости подразумевает комбинированное лечение, первым этапом которого является хирургический метод. Большинство хирургических методов не являются персонализированными и основаны на резекции языка, затрагивающей больше половины органа, что приводит к существенному функциональному дефициту и инвалидизации пациентов.
Цель. На серии клинических случаев продемонстрировать возможность устранения дефектов языка с применением предоперационного компьютерного 3D-планирования.
Материалы и методы. За период с 2021 по 2024 г. в условиях отделения ЧЛХ ФГБУ НМИЦО ФМБА России с применением компьютерного цифрового 3D-планирования были прооперированы 4 пациента (3 мужчин и 1 женщина) с первичным раком боковой поверхности языка. Средний возраст больных составил 53 года. Средний период наблюдения 14 мес, за период наблюдения ни у одного пациента не было отмечено продолженного роста или рецидива новообразования. Пациенты были представлены со стадиями рТ1–рТ4, без поражения регионарных лимфатических узлов (N0). Пациентам на предоперационном этапе проведены инструментальные и клинико-лабораторные исследования по стандартизированному протоколу. Для оценки эффективности лечения и качества жизни все пациенты на предоперационном и постоперационном этапах были анкетированы по опросникам Европейской организации по исследованию и лечению рака головы и шеи.
Компьютерное моделирование оперативного вмешательства осуществлялось в программах Slicer и Blender, печать шаблонов выполнялась на 3D-принтере Elegoo Saturn 2. Произведена оценка функций речи и глотания с использованием протокола Покровского и программного обеспечения Vospector-DSI на предоперационном и постоперационном этапах. Лечащим врачом проводились антропофотометрия и видеофиксация речи пациентов и их жалоб на всех этапах курации.
Результаты. Всем пациентам была выполнена гемиглоссэктомия и профилактическая шейная лимфодиссекция на стороне поражения с одномоментной реконструкцией языка лучевым лоскутом предплечья с использованием предоперационного компьютерного 3D-планирования. Выживаемость лоскутов составила 100% во всей серии наблюдений. Онкологическая радикальность у всех пациентов была обеспечена R0. Среднее время оперативного вмешательства составило 288 мин. Постоперационный период проходил без осложенией, средний период пребывания пациентов в стационаре составил 14 сут, отдаленный период наблюдения — от 6 до 20 мес. У всех пациентов достигнут хороший эстетический результат, акустические параметры речи в пределах нормальных значений, средний коэффициент слоговой разборчивости речи по Покровскому составил 88%. Все пациенты были адаптированы к своей привычной диете и профессиональной деятельности без ограничений. По результатам опросников Европейской организации по исследованию и лечению рака головы и шеи (European organization for research and treatment of cancer (EORTC) quality of life questionnaires for head and neck module (QLQ-H&N35), European Organization for Research and Treatment of Cancer Quality of Life Questionnaire) пациенты оценили качество своей жизни после оперативного лечения как хорошее в трех случаях и отличное в одном случае.
Выводы. Использованный нами алгоритм предоперационного компьютерного 3D-планирования является перспективным. Применение операционных щаблонов позволило достичь адекватной онкологической радикальности, синхронизировать работу двух хирургических бригад, сократить время анестезиологического пособия (среднее время оперативного вмешательства 288 мин) и достичь оптимальных функциональных и эстетических результатов. Ввиду подвижности языка и изменчивости его формы требуется создание новых протоколов предоперационной инструментальной диагностики для стандартизации положения языка в ротовой полости. Данная методика требует дальнейшего совершенствования на большей группе пациентов.
Ключевые слова
Для цитирования:
Хачатрян А.А., Назарян Д.Н., Черненький М.М., Джуганова В.О., Федосов А.В., Захаров Г.К., Потапов М.Б., Данищук О.И., Осипенко Е.В., Михеева Е.И. Современный подход в микрохирургическом устранении дефектов языка с применением компьютерного цифрового планирования. Медицина экстремальных ситуаций. 2024;26(3):98-105. https://doi.org/10.47183/mes.2024-26-3-98-105
For citation:
Khachatryan A.A., Nazarian D.N., Chernenkiy M.M., Dzhuganova V.О., Fedosov A.V., Zakharov G.K., Potapov M.B., Danishuk O.I., Osipenko E.V., Micheeva E.I. Modern approach in microsurgical elimination of tongue defects using computerized digital planning. Extreme Medicine. 2024;26(3):98-105. https://doi.org/10.47183/mes.2024-26-3-98-105
ВВЕДЕНИЕ
Злокачественные новообразования (ЗНО) головы и шеи занимают шестое место в структуре общей онкологической заболеваемости и в 90% случаев представлены плоскоклеточным раком. Рак ротовой полости является самым распространенным злокачественным новообразованием в области головы и шеи. Лидирующей локализацией всех опухолевых образований ротовой полости в 60% случаев является язык с одинаковой частотой поражения как правой, так и левой его половины [1–3]. В структуре онкологических заболеваний в период 2013–2020 гг. в России заболеваемость ЗНО слизистой полости рта составила по разным источникам порядка 1,9% [4].
Одним из основных способов лечения злокачественных новообразований слизистой оболочки ротовой полости на первом этапе является хирургический метод. Резекция даже части языка приводит к существенному функциональному снижению качества жизни и значительно влияет на процесс глотания и речеобразования [5–10]. «Золотым стандартом» в лечении пациентов с дефектами языка является применение свободных реваскуляризированных лоскутов на микрососудистых анастомозах [5][10][11].
В 1981 г. Yang описал способ применения кожно-фасциального лучевого лоскута предплечья (radial fasciocutaneous forearm falp) для устранения дефектов различных областей тела человека. В арсенале использования у реконструктивных хирургов этот способ стабильно занял свое место. Лоскут представляет собой тонкий пластичный материал с постоянной сосудистой анатомией и длинной сосудистой ножкой. В реконструкции языка лоскут применяется при дефектах, образующихся после гемиглоссэктомий; для увеличения его объема забор может быть осуществлен с дополнительным количеством жировой ткани предплечья. Более того, за счет кожного нерва предплечья может быть осуществлена чувствительная реиннервация лоскута [12].
Описано множество техник выкройки кожно-фасциального лоскута предплечья (методика «snoopy head», билобарные лоскуты) и адаптации лоскута к краям дефекта [13]. Однако данные способы не могут называться персонализированными в связи с тем, что они не поддаются математическому анализу и не содержат информации о заранее необходимых параметрах лоскута. Применение цифровых технологий в реконструктивной хирургии языка позволяет получить прогнозируемый и стандартизированный результат, способствующий сокращению операционного времени вмешательства за счет возможности одновременной работы двух бригад [14].
Использование резекционных 2D-шаблонов-трафаретов, выкраиваемых интраоперационно, чаще всего из бумаги, при планировании забора мягкотканных аутотрансплантатов имеет свои недостатки, а именно: невозможность заблаговременного проектирования шаблона в связи с тем, что создание трафарета происходит после иссечения опухолевого образования и визуализации дефекта языка и основано только на зрительном контроле хирурга. Данный момент обусловливает удлинение анестезиологического и операционного пособия ввиду невозможности одномоментной работы двух хирургических бригад. Недостатком методики 2D также является отсутствие информации на дооперационном этапе о планируемом объеме резекции языка и размере опухоли. Это связано с тем, что до хирургического вмешательства невозможно определить последующую потерю объема языка, связанную с проведением лучевой терапии и/или атрофией лоскута [15][16]. Для решения этой задачи нами предложен и апробирован способ устранения дефектов языка мягкотканным лоскутом у онкологических больных, нуждающихся в резекции языка с одномоментной реконструкцией языка, на основании компьютерного 3D-планирования и создания резекционных шаблонов. Научная новизна подтверждена патентом на изобретение в России № 2024104882 «Способ устранения дефектов языка после частичной глоссэктомии», опубликованным 04.07.2024.
Цель исследования — на серии клинических случаев продемонстрировать возможность устранения дефектов языка с применением предоперационного компьютерного 3D-планирования.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2021 по 2024 г. в условиях отделения ЧЛХ НМИЦО ФМБА России по методике микрохирургического устранения дефектов языка с применением компьютерного цифрового 3D-планирования были прооперированы 4 пациента: трое мужчин и одна женщина с диагнозом «первичный рак боковой поверхности языка». Пациенты были представлены со стадиями развития опухолевого процесса рТ1–рТ4а, без поражения регионарных лимфатических узлов (N0), подтвержденными результатами гистологического исследования. Средний возраст больных составил 53 года. Всем пациентам была выполнена гемиглоссэктомия и профилактическая шейная лимфодиссекция на стороне поражения с одномоментной реконструкцией языка лучевым лоскутом предплечья. Сводные данные пациентов указаны в таблице 1.
Инструментальные методы исследования на предоперационном этапе включали: магнитно-резонансную томографию мягких тканей челюстно-лицевой области с контрастным усилением (МРТ ЧЛО с КУ) для выяснения стадии процесса по критерию Т (международной классификации онкологических опухолей) и оценки распространения опухолевого процесса в тканях языка, мультиспиральную компьютерную томографию челюстно-лицевой области с контрастным усилением (МСКТ ЧЛО с КУ) для выбора реципиентных сосудов, определения сосудистого тока бассейна наружной сонной артерии и исключения внутрисосудистых патологий (окклюзии, тромбоза), мультиспиральную компьютерную томографию донорской области (предплечье) с контрастным усилением (МСКТ с КУ) для учета диаметра основных магистральных сосудов, выявления аномалий сосудистого русла и анатомических особенностей сосудов, ультразвуковую доплерографию сосудов брахиоцефального ствола и сосудов донорской области (УЗДГ). Для выбора донорской зоны (предплечье верхней конечности) проведена клиническая оценка проходимости артерий и коллатерального кровоснабжения кисти тестом Аллена. Для оценки функции глотания всем пациентам была выполнена трансназальная эндоскопическая ларингоскопия с глотательными пробами (трехглотковый тест) с видеофиксацией.
Все пациенты на предоперационном и постоперационном этапах были анкетированы по опросникам оценки качества жизни, рекомендованным Европейской организацией по исследованию и лечению рака головы и шеи (European organization for research and treatment of cancer (EORTC) quality of life questionnaires for head and neck module (QLQ-H&N35), European Organization for Research and Treatment of Cancer Quality of Life Questionnaire), с дополнительно включенными шкалами MD Doctor of medicine Anderson и The Voice Handicap Index (VHI-10), которые имеют более высокую специфичность для пациентов, перенесших лечение по поводу орофарингеального рака. Анкетирование проводилось на догоспитальном этапе и при каждом контрольном посещении через 1, 3, 6 и 12 мес. Пациентам с обильным волосяным покровом в области донорской зоны была проведена лазерная эпиляция на догоспитальном этапе. Оценка функций речи и глотания выполнялась штатным фониатром, специалистом по речи и глотанию с использованием протокола Покровского и программного обеспечения Vospector-DSI на предоперационном и постоперационном этапах [19]. Лечащим врачом проводилась антропофотометрия и видеофиксация речи пациентов и их жалоб на всех этапах курации. Тактика лечения для всех пациентов определялась на онкологическом консилиуме на базе Федерального медицинского биофизического центра имени А.И. Бурназяна. Компьютерное моделирование оперативного вмешательства проводилось с использованием программного обеспечения Slicer и Blender, печать шаблонов осуществлялась на 3D-принтере Formlab 3.
Таблица 1. Сводные данные пациентов
|
Данные пациентов |
Пациенты |
|||
|
1 |
2 |
3 |
4 |
|
|
Пол |
Мужской |
Мужской |
Мужской |
Женский |
|
Возраст, лет |
40 |
50 |
50 |
70 |
|
Локализация опухоли |
Правая боковая поверхность языка |
Левая боковая поверхность языка |
Правая боковая поверхность языка, корень языка |
Правая боковая поверхность языка |
|
Стадия опухолевого процесса по TNM* |
рТ2N0M0 |
рТ2N0M0 |
рТ4аN0M0 |
рТ1N0M0 |
|
Особенность резекции |
Резекция правой боковой поверхности языка с сохранением кончика и корня языка |
Резекция левой боковой поверхности языка с сохранением кончика и корня языка |
Резекция правой боковой поверхности, кончика и корня языка |
Резекция правой боковой поверхности языка с сохранением кончика и корня языка |
|
Процент резекции от объема языка, % |
40 |
40 |
60 |
40 |
|
Размеры лоскута длина/ширина, мм |
50/40 |
57/72 |
71/65 |
60/40 |
|
Время забора лоскута, мин |
125 |
115 |
90 |
130 |
|
Время резекции, мин |
80 |
92 |
97 |
82 |
|
Время оперативного вмешательства, мин |
310 |
270 |
295 |
280 |
|
Время госпитализации, койко-дни |
13 |
14 |
15 |
14 |
|
Срок удаления назогастрального зонда, сут |
12 |
12 |
12 |
12 |
|
Индекс Покровского, % |
93 |
– |
73 |
95 |
|
Послеоперационные осложнения |
Венозный стаз лоскута |
нет |
нет |
нет |
|
Период наблюдения, мес. |
21 |
16 |
16 |
6 |
|
Онкологический статус |
Безрецидивное течение |
Безрецидивное течение |
Безрецидивное течение |
Безрецидивное течение |
|
Статус пациента на момент публикации статьи |
жив |
жив |
жив |
жив |
|
Оценка качества жизни по самоопроснику (от 1 до 7 баллов) |
6 (хорошо) |
6 (хорошо) |
6 (хорошо) |
7 (отлично) |
Таблица составлена авторами по собственным данным
Примечание: * TNM — международная классификация онкологических опухолей, где T (tumor — опухоль) распространенность первичной опухоли, N (nodus — узел) наличие, отсутствие и распространенность метастазов в регионарных лимфатических узлах, M (отделенные метастазы), наличие или отсутствие отделенных метастазов.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
За неделю до оперативного вмешательства было выполнено компьютерное предоперационное планирование на основании данных МСКТ ЧЛО, МРТ ЧЛО и МСКТ верхних конечностей. Для этого посрезово контурировались ткани языка с шагом в 5–7 срезов.
Далее на основании методов математической интерполяции с использованием программного обеспечения Slicer и Blender определялся выделенный объем образования с учетом отступа от границ опухоли 1,5 см для достижения краев границ резекции R0. Полученные данные преобразовывались в площадь поверхности и адаптировались к рельефу донорской руки, размещая поверхность шаблона-трафарета над осевыми сосудами (лучевые сосуды) для включения их в лоскут. Площадь поверхности лоскута увеличивали на 15% с учетом возможного сокращения лоскута после проведения лучевой терапии. Таким образом изготавливались два шаблона: резекционный, по которому проводилась гемиглоссэктомия, и шаблон-трафарет, по которому осуществлялась выкройка кожной площадки лучевого лоскута (рис. 1).
После согласования предоперационного планирования с оперирующими хирургами цифровой проект в виде STL (стереолитографической) модели отправлялся в печать на 3D-принтере Elegoo Saturn 2. Среднее время печати шаблонов занимало 40–50 мин.
Оперативные вмешательства проводились двумя бригадами хирургов по стандартному протоколу. Первая бригада хирургов выполняла абляцию опухоли языка с применением резекционного шаблона, шейную лимфодиссекцию, выделение реципиентных сосудов шеи (рис. 2).
Каждому пациенту была выполнена экстренная интраоперационная биопсия краев (6 препаратов) резекции, во всех случаях края резекции R0 (рис. 3).
Вторая бригада хирургов симультанно выделяла лучевой лоскут с использованием шаблона-трафарета. Среднее время резекционного этапа составляло 87 мин. Среднее время забора лоскута — порядка 115 мин. Выделение лучевого лоскута во всех случаях осуществлялось с включением в лоскут лучевой артерии и комитантных вен, а также латерального кожного нерва предплечья (рис. 4). После выделения лоскута проводилось отсечение сосудистой ножки трансплантата и перемещение трансплантата в ротовую полость.
Кожная площадка лоскута фиксировалась к оставшейся части языка наводящими швами, донорские сосуды проводились в тоннеле, сформированном в мягких тканях дна полости рта, после чего осуществлялся микрохирургический этап. Во всех случаях выполнялось анастомозирование лучевой артерии с лицевой артерией по типу анастомоза «конец в конец», аналогично анастомозировались комитантные вены с наружной яремной веной. На завершающем этапе выполнялась нейрорафия латерального кожного нерва и язычного нерва в двух случаях и подъязычного нерва (по типу «конец в бок») в двух случаях. Среднее время микрохирургического этапа составило 45 мин. После пуска кровотока оценивалось наполнение донорских сосудов визуально и при помощи портативного доплера «Минидоп» («Биосс»). Лоскут адаптировали к оставшейся части языка резорбируемой нитью Викрил 3.0, после чего выполнялось послойное ушивание ран (рис. 5).
Послеоперационный период у большинства пациентов протекал без особенностей. Только у одного пациента спустя 3 ч после оперативного вмешательства отмечался венозный стаз лоскута, в связи с чем была проведена ревизионная операция с повторным выполнением венозных анастомозов. В дальнейшем у данного пациента послеоперационный период проходил без особенностей. Назогастральный зонд был удален у всех пациентов на 12-е сут, средний период пребывания пациентов в стационаре составил 14 сут (рис. 6).
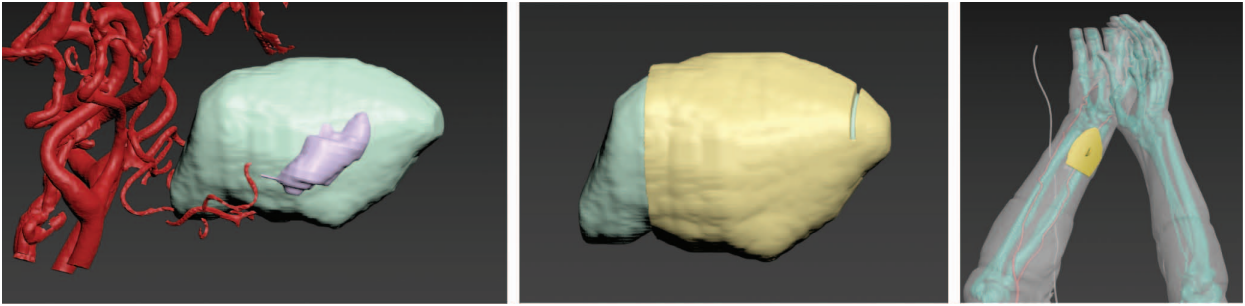
Рисунок подготовлен авторами
Рис. 1. Предоперационное компьютерное 3D-планирование
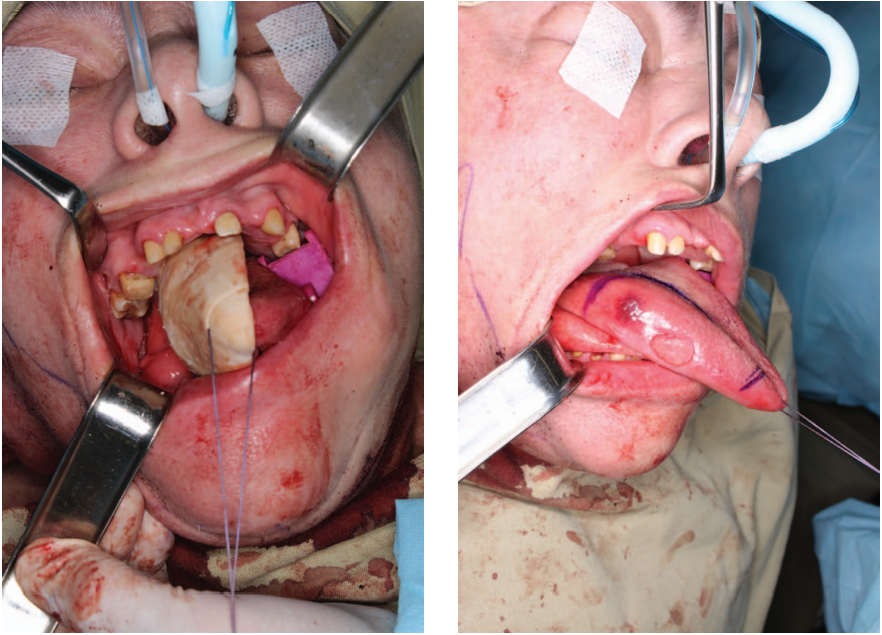
Рисунок подготовлен авторами
Рис. 2. Маркировка зоны резекции с использованием резекционного шаблона, визуализируется злокачественное новообразование языка, поражающее его боковую поверхность
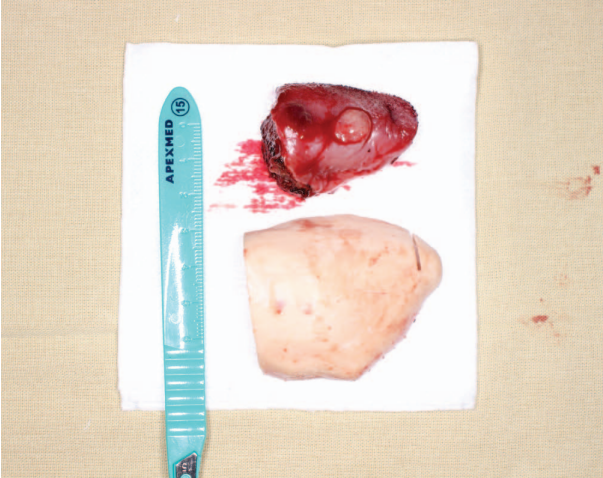
Рисунок подготовлен авторами
Рис. 3. Удаленный препарат языка
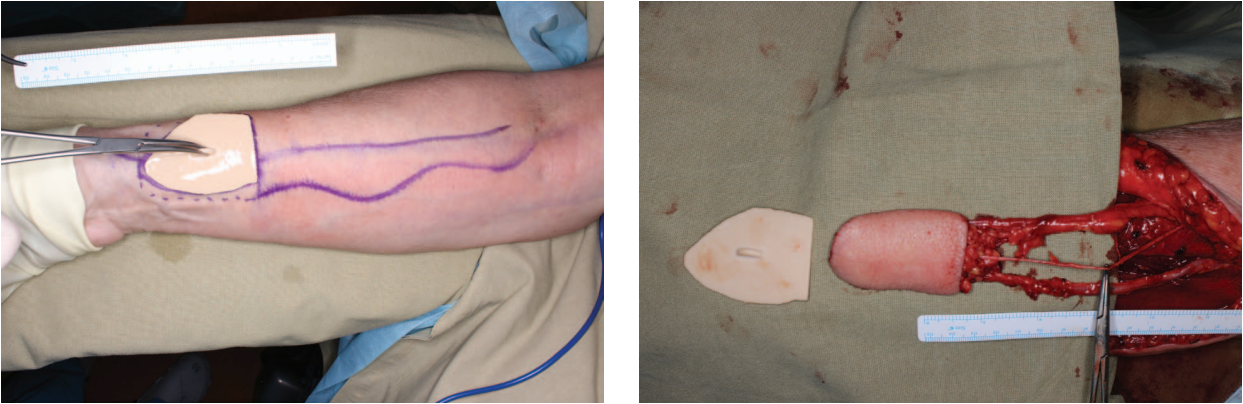
Рисунок подготовлен авторами
Рис. 4. Маркировка лоскута с применением шаблона-трафарета. Лучевой лоскут на сосудистой ножке
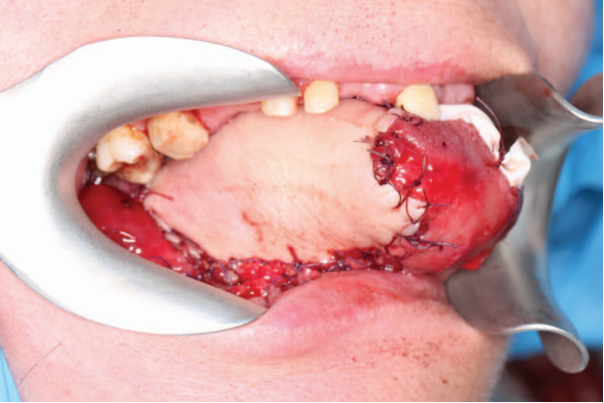
Рисунок подготовлен авторами
Рис. 5. Вид лоскута после ушивания раны и запуска кровотока
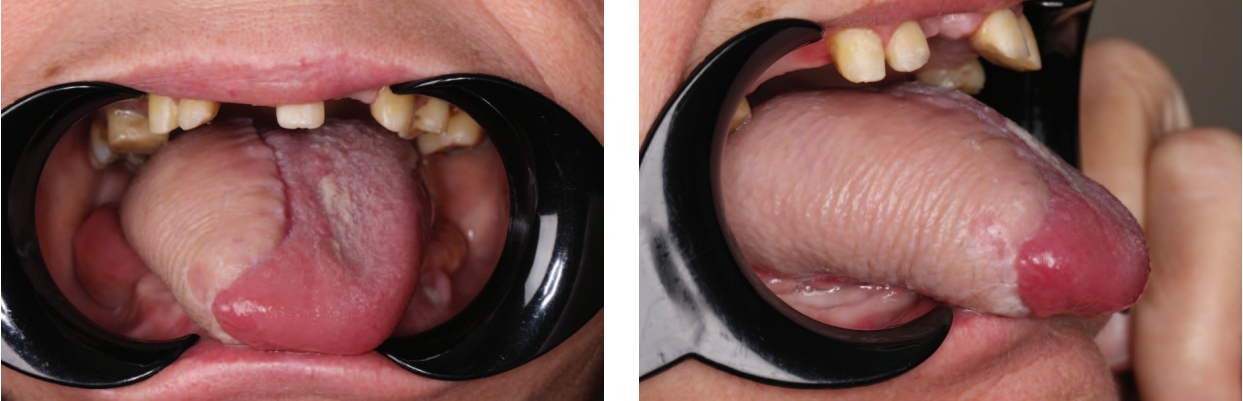
Рисунок подготовлен авторами
Рис. 6. Антропофотометрия через месяц после операции
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В настоящее время компьютерное моделирование широко применяется в реконструктивной челюстно-лицевой хирургии для устранения костных дефектов челюстно-лицевой области, позволяя производить сложные реконструктивные операции с заранее прогнозируемым результатом. Однако в устранении мягкотканных дефектов челюстно-лицевой области применение хирургических шаблонов остается малоизученным. Сложность применения данной методики и планирования мягкотканных аутотрансплантатов заключается в отсутствии стабильных опорных костных элементов, необходимости восстановления не только объема тканей, но и обеспечения их должной мобильности [14].
Первое применение резекционных шаблонов, а именно резекционных 2D-шаблонов-трафаретов, при планировании забора мягкотканных аутотрансплантатов для восполнения дефицита тканей языка было впервые описано R.M. Baskin и соавт. [15].
Необходимо отметить, что в отечественной литературе результаты применения компьютерного планирования и шаблонной хирургии для устранения мягкотканных дефектов языка и дна полости рта не описаны, а в зарубежной литературе нами было найдено лишь две оригинальные статьи, освещающие данную проблематику [16][17].
Наиболее близким к апробированному нами подходу является метод, представленный H. Koumoullis, который впервые предложил способ использования 3D-моделирования и шаблонной хирургии для осуществления реконструкции языка после глоссэктомии с использованием персонализированного пациент-ориентированного планирования реконструкции мягких тканей (Personalised pAtient-specific plaNning of SOFt tissue reconstruction) PANSOFOS [16]. Автор отмечал возможность индивидуальной реконструкции мягких тканей головы и шеи мягкотканным аутотрансплантатом с использованием 3D-планирования. При этом недостатком предложенной им методики являлась невозможность на дооперационном этапе прогнозирования планируемого объема резекции языка и установления потери объема органа после лучевой терапии и/или атрофии лоскута.
В исследованиях H. Lu, J. Qin, R. Yue, C. Liu и соавт. описан метод визуализации опухоли с использованием данных компьютерной томографии для выполнения прецизионной резекции опухолей средней линии языка без нарушения кровотока по лицевым артериям. Однако данная методика не подразумевала применения хирургических шаблонов [17].
P. Sinha и соавторы предложили метод визуализации опухоли языка путем печати на 3D-принтере физической модели языка пациента с выделением альтернативным цветом опухоли на предоперационнном этапе, что позволяет хирургам лучше оценить степень распространения опухолевого процесса. Однако данный подход не включал в себя изготовления ни резекционных шаблонов, ни шаблонов для выкройки свободного лоскута [18].
При апробации вышеописанного подхода (предоперационного планирования мягкотканных реконструктивных аутотрансплантатов) нами и рядом авторов [19] отмечено существенное уменьшение времени оперативного вмешательства, что значительно снижает интраоперационные риски для пациента и уменьшает финансовые затраты на анестезиологическое пособие.
Описанный нами подход устранения дефекта языка после удаления злокачественного новообразования с применением компьютерного цифрового планирования позволяет точно (с погрешностью 0,2 мм) определить границы опухоли, предварительно выполнив оперативное вмешательство в цифровом поле. Для обеспечения необходимой онкологической радикальности (чистых краев) резекционный шаблон включает в себя такой параметр, как онкологический отступ в 1,5 см от опухоли. Трафарет для выкройки кожно-фасциального лоскута, созданный с учетом объема резецируемой части языка, имеет увеличенный на 15% объем для нивелирования постоперационного рубцевания и сокращения объема лоскута.
Несмотря на наличие современных протоколов подавления артефактов от металлических ортопедических реставраций при проведении лучевых методов диагностики головы и шеи, не у всех пациентов удавалось достичь объективной картины визуализации мягких тканей языка и дна полости рта. У большинства наших пациентов на момент обращения в ротовой полости имелись металлические ортопедические конструкции (золото, кобальт-хромовый сплав). С целью нивелирования артефактов при лучевых методах диагностики (МРТ, МСКТ) после клинического осмотра ротовой полости штатным стоматологом-ортопедом выполнялось удаление всех металлических ортопедических конструкций и замена их на пластмассовые коронки.
Проблема подвижности языка и изменения его объема из-за сокращения мышц на этапе лучевой диагностики остается важной задачей, решение которой будет представлено в последующих исследованиях. Для стандартизации предоперационного планирования представляется актуальной необходимость создания специализированных протоколов положения языка в ротовой полости на диагностических этапах.
ЗАКЛЮЧЕНИЕ
Предложенная нами методика компьютерного 3D-планирования является перспективной и реализует возможность точного проектирования предоперационного плана хирургического вмешательства. Данный подход демонстрирует возможность применения операционных шаблонов для достижения адекватной онкологической радикальности (за счет заранее спланированной зоны резекции), синхронизации работы двух хирургических бригад, сокращения времени анестезиологического пособия (среднее время оперативного вмешательства 288 мин), что позволяет достичь хороших функциональных и эстетических результатов. Применение резекционного шаблона позволяет удалить новообразование в соответствии с онкологическими принципами, а шаблон-трафарет — точно обозначить форму и объем свободного микрохирургического лоскута, который в дальнейшем используется для устранения дефекта языка. Ввиду подвижности языка и изменчивости его формы требуется создание новых протоколов предоперационной инструментальной диагностики для стандартизации положения органа в ротовой полости. Данный подход хирургического вмешательства является перспективным направлением, однако требует усовершенствования и апробации на большей группе пациентов ввиду поиска новых реконструктивных операций с целью улучшения функциональных результатов, снижения травматичности без ущерба онкологической радикальности. В настоящее время очевидна необходимость дальнейшего развития указанного направления.
Список литературы
1. Sarode G, Maniyar N, Sarode SC, Jafer M, Patil S, Awan KH. Epidemiologic aspects of oral cancer. Dis Mon. 2020;66(12):100988. https://doi.org/10.1016/j.disamonth.2020.100988
2. Kumar M, Nanavati R, Modi TG, Dobariya C. Oral cancer: Etiology and risk factors: A review. J Cancer Res Ther. 2016;12(2):458–63. https://doi.org/10.4103/0973-1482.186696
3. Stepan KO, Mazul AL, Larson J, Shah P, Jackson RS, Pipkorn P, et al. Changing Epidemiology of Oral Cavity Cancer in the United States. Otolaryngol Head Neck Surg. 2023;168(4):761–8. https://doi.org/10.1177/01945998221098011
4. Рыхлевич АА. Общая заболеваемость злокачественными новообразованиями слизистой полости рта в Российской Федерации за 2013–2020 годы. Современные проблемы здравоохранения и медицинской статистики. 2022;4:689–705. https://doi.org/10.24412/2312-2935-2022-4-689-705
5. Yi CR, Jeong WS, Oh TS, Koh KS, Choi JW. Analysis of speech and functional outcomes in tongue reconstruction after hemiglossectomy. Journal of Reconstructive Microsurgery. 2020;36:507–13. https://doi.org/10.1055/s-0040-1709493
6. Engel H, Huang JJ, Lin CY, Lam W, Kao HK, Gazyakan E, Cheng MH. A strategic approach for tongue reconstruction to achieve predictable and improved functional and aesthetic outcomes. Plast Reconstr Surg. 2010;126(6):1967–77. https://doi.org/10.1097/PRS.0b013e3181f44742
7. Lam L, Samman N. Speech and swallowing following tongue cancer surgery and free flap reconstruction--a systematic review. Oral Oncol. 2013;49(6):507–24. https://doi.org/10.1016/j.oraloncology.2013.03.001
8. Chang EI, Yu P, Skoracki RJ, Liu J, Hanasono MM. Comprehensive analysis of functional outcomes and survival after microvascular reconstruction of glossectomy defects. Ann Surg Oncol. 2015;22(9):3061–9. https://doi.org/10.1245/s10434-015-4386-6
9. Ihara Y, Tashimo Y, Nozue S, Iizumi Y, Fukunishi Y, Saito Y, Shimane T, Takahashi K. Changes in Oral Function and Quality of Life in Tongue Cancer Patients Based on Resected Area. Asian Pac J Cancer Prev. 2021;22(8):2549–57. https://doi.org/10.31557/APJCP.2021.22.8.2549
10. Gilbert RW. Reconstruction of the oral cavity; past, present and future. Oral Oncol. 2020;108:104683. https://doi.org/10.1016/j.oraloncology.2020.104683
11. Haughey BH. Tongue reconstruction: concepts and practice. Laryngoscope. 1993;103(10):1132–41. https://doi.org/10.1288/00005537-199310000-00010
12. Chepeha DB, Teknos TN, Shargorodsky J, Sacco AG, Lyden T, Prince ME, Bradford CR, Wolf GT. Rectangle tongue template for reconstruction of the hemiglossectomy defect. Arch Otolaryngol Head Neck Surg. 2008;134(9):993–8. https://doi.org/10.1001/archotol.134.9.993
13. Absolon KB, Rogers W, Aust JB. Some historical developments of the surgical therapy of tongue cancer from the seventeenth to the nineteenth century. Am J Surg. 1962;104:686–91. https://doi.org/10.1016/0002-9610(62)90419-1
14. Jacek B, Maciej P, Tomasz P, Agata B, Wiesław K, Radosław W, et al. 3D printed models in mandibular reconstruction with bony free flaps. J Mater Sci Mater Med. 2018;29(3):23–5. https://doi.org/10.1007/s10856-018-6029-5
15. Baskin RM, Seikaly H, Sawhney R, Danan D, Burt M, Idris S, et al. Tongue reconstruction: Rebuilding mobile three-dimensional structures from immobile two-dimensional substrates, a fresh cadaver study. Head Neck. 2019;41(10):3693–99. https://doi.org/10.1002/hed.25889
16. Koumoullis H, Burley O, Kyzas P. Patient-specific soft tissue reconstruction: an IDEAL stage I report of hemiglossectomy reconstruction and introduction of the PANSOFOS flap. Br J Oral Maxillofac Surg. 2020;58(6):681–6. https://doi.org/10.1016/j.bjoms.2020.04.017
17. Lu H, Qin J, Yue R, Liu C, Li S, Wu D. Application of 3D reconstruction for midline glossectomy in OSA patients. Eur Arch Otorhinolaryngol. 2020;277(3):925–31. https://doi.org/10.1007/s00405-020-05783-5
18. Sinha P, Bylapudi BP, Puranik P, Subash A, Rao V. 3D Patient-Specific Biomechanical Model of the Tongue for the Management of Tongue Tumors: Conceptualization to Reality. Sisli Etfal Hastan Tip Bul. 2022;56(4):559–63. https://doi.org/10.14744/SEMB.2022.37039
19. McCarty JL, Corey AS, El-Deiry MW, Baddour HM, Cavazuti BM, Hudgins PA. Imaging of Surgical Free Flaps in Head and Neck Reconstruction. AJNR Am J Neuroradiol. 2019;40(1):5–13. https://doi.org/10.3174/ajnr.A5776
20. Покровский НБ. Расчет и измерение разборчивости речи. Связьиздат 1962;392.
Об авторах
А. А. ХачатрянРоссия
Хачатрян Арбак Арманович
Москва
Д. Н. Назарян
Россия
Назарян Давид Назаретович, д-р мед. наук
Москва
М. М. Черненький
Россия
Черненький Михаил Михайлович
Москва
В. О. Джуганова
Россия
Джуганова Виктория Олеговна
Москва
А. В. Федосов
Россия
Федосов Александр Викторович
Москва
Г. К. Захаров
Россия
Захаров Георгий Карленович
Москва
М. Б. Потапов
Россия
Потапов Максим Борисович
Москва
О. И. Данищук
Россия
Данищук Ольга Игоревна
Москва
Е. В. Осипенко
Россия
Осипенко Екатерина Владимировна, канд. мед. наук
Москва
Е. И. Михеева
Россия
Михеева Евгения Игоревна
Москва
Дополнительные файлы
Рецензия
Для цитирования:
Хачатрян А.А., Назарян Д.Н., Черненький М.М., Джуганова В.О., Федосов А.В., Захаров Г.К., Потапов М.Б., Данищук О.И., Осипенко Е.В., Михеева Е.И. Современный подход в микрохирургическом устранении дефектов языка с применением компьютерного цифрового планирования. Медицина экстремальных ситуаций. 2024;26(3):98-105. https://doi.org/10.47183/mes.2024-26-3-98-105
For citation:
Khachatryan A.A., Nazarian D.N., Chernenkiy M.M., Dzhuganova V.О., Fedosov A.V., Zakharov G.K., Potapov M.B., Danishuk O.I., Osipenko E.V., Micheeva E.I. Modern approach in microsurgical elimination of tongue defects using computerized digital planning. Extreme Medicine. 2024;26(3):98-105. https://doi.org/10.47183/mes.2024-26-3-98-105

















