Перейти к:
Противосудорожная активность оригинальных аминоэфиров вальпроевой кислоты при интоксикации ингибитором холинэстераз
https://doi.org/10.47183/mes.2025-327
Аннотация
Введение. Наиболее распространенной причиной острых интоксикаций, сопровождающихся развитием судорожного синдрома, являются ингибиторы холинэстераз в составе бытовой химии, агрохимикатов и ряда лекарственных средств. Отсроченное и повторное применение существующих антидотов малоэффективно. К соединениям, перспективным для разработки альтернативных средств терапии, относятся производные вальпроевой кислоты.
Цель. Оценка противосудорожной эффективности оригинальных аминоэфиров вальпроевой кислоты при интоксикации ингибитором холинэстеразы — фенилкарбаматом.
Материалы и методы. Эксперименты проведены на беспородных белых крысах-самцах возрастом 3 месяца и массой тела 200– 240 г. При определении средних летальных доз новых соединений использовали табличный экспресс-метод по В.Б. Прозоровскому.
Для моделирования судорожного синдрома внутрибрюшинно вводили крысам-самцам фенилкарбамат в дозе 1 мг/кг м.т. Оценивали противосудорожную активность аминоэфиров вальпроевой кислоты: N-метил-4-пиперидинольный (АВК), хинуклидинольный (ХАВК) и тропиновый (ТАВК), вводимые в дозах 21,5 и 43 мг/кг м.т. после начала судорог. Исследование проведено на 4 опытных группах: фенилкарбамат «Ф» (n = 8), Ф+АВК (n = 16), Ф+ТАВК (n = 16), Ф+ХАВК (n = 16). Исследуемые субстанции растворяли в 0,9%-ном растворе хлорида натрия и вводили внутрибрюшинно, с учетом межвидового пересчета доз. Объем вводимого внутрибрюшинно раствора составлял 0,1 мл/100 г. Выраженность судорожного синдрома в эксперименте оценивали по шкале Racine. Учитывали показатели эффективности: латентный период, выраженность и продолжительность судорожного синдрома, летальность. Статистическую обработку результатов исследования производили с помощью пакета программы Statistica 13.0 (Statsoft, США).
Результаты. Установленные значения ЛД50 оригинальных аминоэфиров вальпроевой кислоты соответствуют 3-му классу умеренно токсичных веществ. В дозе 21,5 мг/кг м.т. значимо уменьшалась доля крыс с выраженными судорогами во всех группах, наиболее быстрый противосудорожный эффект регистрировали в группе ХАВК (через 10 мин судороги отсутствовали). Эффективность АВК и ТАВК при использовании в дозе 43 мг/кг м.т. была сопоставима с дозой 21,5 мг/кг м.т., в группе ХАВК через 10 мин доля животных с судорогами оставалась высокой. Достоверное уменьшение продолжительности судорог выявлено в группе ХАВК в дозах 21,5 и 43 мг/кг м.т. Достоверное снижение интенсивности судорог выявлено в группах АВК и ХАВК в дозе 21,5 мг/кг м.т., группах АВК и ТАВК — в дозе 43 мг/кг м.т.
Выводы. Новые аминоэфиры вальпроевой кислоты проявляют противосудорожную активность при интоксикации обратимым ингибитором холинэстераз. В дозе 21,5 мг/кг м.т. наиболее эффективен ХАВК, однако в дозе 43 мг/кг м.т. наблюдаются проявления токсичности и более эффективен АВК. Несмотря на летальность животных, ТАВК также проявляет свою эффективность в дозе 43 мг/кг м.т.
Ключевые слова
Для цитирования:
Бельская А.В., Мелехова А.С., Зорина В.Н., Беспалов А.Я., Мельникова М.В., Бондаренко А.А. Противосудорожная активность оригинальных аминоэфиров вальпроевой кислоты при интоксикации ингибитором холинэстераз. Медицина экстремальных ситуаций. 2025;27(4):453-461. https://doi.org/10.47183/mes.2025-327
For citation:
Belskaya A.V., Melekhova A.S., Zorina V.N., Bespalov A.Ya., Melnikova M.V., Bondarenko A.A. Anticonvulsant activity of original valproic acid aminoethers in cholinesterase inhibitor poisoning. Extreme Medicine. 2025;27(4):453-461. https://doi.org/10.47183/mes.2025-327
ВВЕДЕНИЕ
Основной причиной развития генерализованного судорожного синдрома токсической этиологии по-прежнему являются отравления ингибиторами холинэстераз. К веществам данной группы относятся необратимые ингибиторы, в первую очередь фосфорорганические соединения (ФОС), и обратимые ингибиторы, преимущественно производные карбаминовой кислоты (карбаматы). Карбаматы и ФОС входят в состав агрохимии и бытовой химии (пестициды, инсектициды), используются при производстве пластификаторов и полимерных материалов. Карбаматы активно применяются и в фармацевтической промышленности в составе лекарственных средств [1][2]. Количество пострадавших от отравления ингибиторами холинэстераз (бытовые отравления, отравления агрохимикатами, передозировка лекарственных средств, суициды) составляет в мире по нескольку миллионов в год.
Токсическое воздействие ингибиторов холинэстераз на организм приводит к развитию миоза, бронхоспазма, гиперсекреции, рвоты, аритмии и дыхательной недостаточности, являющихся результатом усиленной мускариновой и никотиновой стимуляции на фоне ингибирования активности ацетилхолинэстеразы (АХЭ), способствующей накоплению ацетилхолина в синапсах нейронов и развитию холинергического синдрома [3]; дополнительно ингибируются бутирилхолинэстераза, карбоксилэстераза и некоторые другие ферменты [1][4][5]. Проявления интоксикации со стороны центральной нервной системы включают генерализованные судорожные припадки, которые могут длиться более 30 мин и сопровождаться выраженным повреждением нейронов и представителей нейроглиального окружения головного мозга. Далее холинергические проявления дополняются глутаматергической эксайтотоксичностью, прогрессией нейровоспаления и нейродегенерацией, у пострадавших могут длительно наблюдаться стойкие неврологические нарушения [6].
Очевидно, что в целях повышения выживаемости при остром отравлении ингибиторами холинэстераз, а также нейропротекции и предотвращения дисфункции центральной нервной системы в отдаленном постинтоксикационном периоде необходимо быстро и эффективно купировать судороги. Однако существующая антидотная терапия предназначена в большей степени для снижения степени тяжести и предотвращения летальных исходов на самых ранних этапах интоксикации (до развития судорог), эффективность ее применения на фоне активно развивающегося или развившегося судорожного синдрома значительно снижается. В частности, атропин [5] воздействует только на мускариновые, но не на никотиновые холинергические рецепторы [6] и наиболее эффективен при профилактическом введении в первые минуты после воздействия. Оксимы (пралидоксим и другие) рекомендованы как профилактические антидоты, и только при отравлении ФОС [4]. Из препаратов бензодиазепинового ряда, взаимодействующих с рецепторами гамма-аминомасляной кислоты (ГАМК), предпочтение отдается мидазоламу, быстрота действия которого определяется высокими пенетрантными свойствами в отношении гематоэнцефалического барьера (ГЭБ) [5]. Их эффективность может существенно снижаться на фоне значительного падения экспрессии субъединиц рецепторов и структурно связанных с ними белков и ферментов, способных взаимодействовать с данными веществами через 10–20 мин после воздействия [6], что значительно повышает процент рефрактерных (нечувствительных к действию антидота) судорог. Все вышеперечисленное определяет необходимость разработки новых эффективных средств купирования судорожного синдрома при отравлении ингибиторами холинэстераз.
Одним из перспективных направлений является разработка противосудорожных средств на основе производных вальпроевой кислоты. Известно, что вальпроевая кислота участвует в пре- и постсинаптической модуляции ГАМК-ергической передачи сигналов, воздействует на натриевые, кальциевые и калиевые каналы, способна повышать внеклеточный уровень серотонина и дофамина в гиппокампе, модулировать нейрогенез и оказывать нейропротекторное действие [7]. Однако эффективная доза антиконвульсанта при генерализованном судорожном синдроме очень велика (более 150 мг/кг м.т.), что ограничивает его применение в качестве антидота, к тому же высокие дозы вальпроевой кислоты отличаются тератогенным эффектом [8].
Для уменьшения эффективной дозы проводятся разработки новых лекарственных средств на основе вальпроевой кислоты. В частности, разработан вальпромид (VPM), действующий как «пролекарство» (вальпроевая кислота высвобождается в процессе гидролиза в желудке) [8, 9]. При этом VPM рекомендован к применению только при биполярных расстройствах (не как противосудорожное средство) и одобрен только во Франции и Италии (Depamide®) [9]. Разработан валноктамид (VCD) — изомер вальпромида, обладающий собственной терапевтической активностью (биотрансформация с выделением вальпроевой кислоты в организме минимальна). На данный момент VCD входит в состав седативных средств и как противосудорожное средство прошел только фазу IIb клинических испытаний [8]. Синтезирован секбутилпропилацетамид (SPD) — гомолог VCD, показавший в доклинических исследованиях высокую противосудорожную активность на различных экспериментальных моделях, в том числе и в случаях бензодиазепин-резистентных судорог [8]. Эффективность SPD обусловлена значительно большей скоростью проникновения через гематоэнцефалический барьер (в 12 раз быстрее, чем вальпроевая кислота), продемонстрировано, что SPD обеспечивал сохранение когнитивных функций и уменьшал повреждение нейронов [10]. Однако SPD и VCD малорастворимы в воде и применяются в виде эмульсии [11], что неудобно для применения в качестве антидота. Все вышеперечисленные производные вальпроевой кислоты не зарегистрированы в качестве средств купирования генерализованного судорожного синдрома.
Цель исследования — сравнительное изучение противосудорожной эффективности оригинальных субстанций аминоэфиров вальпроевой кислоты при отравлении ингибитором холинэстеразы — фенилкарбаматом.
МАТЕРИАЛЫ И МЕТОДЫ
Оригинальные производные вальпроевой кислоты были разработаны и синтезированы на базе лаборатории синтеза лекарственных препаратов ФГБУ НКЦТ им. С.Н. Голикова ФМБА России. Перечень и структурные формулы тестируемых субстанций представлены в таблице 1.
При проведении экспериментов в качестве тест-системы были использованы беспородные белые крысы-самцы возрастом 3 мес. и массой тела 200–240 г, поступившие из питомника НИЦ «Курчатовский институт» — ПЛЖ «Рапполово», Ленинградская область. Животных содержали в стандартных условиях в соответствии с правилами1.
На первом этапе проводили оценку острой токсичности и определение средней летальной дозы ТАВК (тропиновый аминоэфир вальпроевой кислоты) и ХАВК (хинуклидинольный аминоэфир вальпроевой кислоты) с использованием экспресс-метода по В.Б. Прозоровскому [12]. Для исследования каждого из соединений экспериментальные животные были разделены на 4 группы по 2 крысы в каждой; производили однократное внутрибрюшинное введение исследуемых растворов (субстанции растворяли в 0,9%-ном растворе хлорида натрия). При изучении острой токсичности для субстанций ТАВК и ХАВК были выбраны следующие дозы: ХАВК 63,1, 79,4, 100,0, 126,0 мг/кг; ТАВК 79,4, 100,0, 126,0, 158,0 мг/кг. В ранее проведенных работах была определена ЛД50 для АВК, равная 170 ± 1,2 мг/кг м.т. [13].
На втором этапе изучали фармакологическую активность субстанций на модели судорог, вызванных обратимым ингибитором холинэстераз — гидрохлоридом замещенного 2[(диметиламино)метил] арилдиметилкарбамата (далее — фенилкарбамат) [14]. Фенилкарбамат вводили однократно внутрибрюшинно в дозе 1 мг/кг м.т. [15]. Формировали следующие опытные группы: группа с изолированным введением фенилкарбамата «Ф» как судорожного агента (n = 8), 3 группы с введением «Ф» и последующим введением исследуемых средств коррекции: Ф+АВК (n = 16), Ф+ТАВК (n = 16), Ф+ХАВК (n = 16). Противосудорожную эффективность субстанций АВК, ХАВК и ТАВК оценивали в двух дозах — 21,5 и 43,0 мг/кг м.т. (по 8 животных на каждую дозу исследуемых веществ).
При выборе эффективных доз исследуемых субстанций и режима введения исходили из принятых в клинической практике дозировок и схем применения у человека вальпроата натрия (Конвулекса®). В качестве основы для расчета эффективной дозы взята средняя дозировка — 7 мг/кг м.т. Межвидовой пересчет доз с человека на крыс производили с использованием стандартных рекомендаций А.Н. Миронова2. Расчет величин тестируемых доз осуществляли с использованием коэффициентов: величина терапевтической дозы для крысы составляла 7,0×39 (коэффициент для человека массой 70 кг) / 6,5 (коэффициент для крысы массой 200 г) ≈ 43,0 мг/кг м.т.
Исследуемые субстанции растворяли в 0,9%-ном растворе хлорида натрия и вводили внутрибрюшинно, с учетом межвидового пересчета доз. Объем вводимого внутрибрюшинно раствора составлял 0,1 мл/100 г. Введение осуществляли в первые минуты после начала судорог 3–4-го уровня по шкале Racine [16], вызванных введением ингибитора холинэстераз.
Учитывали показатели эффективности: латентный период, выраженность и продолжительность судорожного синдрома, летальность. Наблюдение и регистрацию смертельных исходов проводили в течение суток. Летальность оценивали по доле погибших крыс от их общего количества в исследуемой группе после введения судорожного агента в течение суток наблюдения. Выраженность судорожного синдрома в эксперименте оценивали по шкале Racine. Судороги 4-го уровня и выше, эквивалентные генерализованным клонико-тоническим судорогам у человека, относили к категории выраженных. Продолжительность судорожного синдрома измеряли в минутах. Для оценки значимости различий в частоте появления крыс с выраженными судорогами использовали точный критерий Фишера. Сравнительную оценку показателей судорожного синдрома у самцов крыс при отравлении фенилкарбаматом проводили с применением критерия Краскела – Уоллиса. Для выявления различий между отдельными группами, а также изучаемых субстанций с группой «Ф» использовали тест множественного сравнения Данна (post-hoc анализ). Статистическую обработку результатов исследования проводили с помощью пакета программы Statistica 13.0 (Statsoft, США).
РЕЗУЛЬТАТЫ
В ходе работы по определению количественных значений характеристик острой токсичности при внутрибрюшинном введении ХАВК было установлено следующее распределение гибели крыс в каждой дозовой подгруппе: 0, 0, 2, 2 особи, что позволило определить величину ЛД50 для ХАВК на уровне 89,8 ± 7,1 мг/кг; при внутрибрюшинном введении ТАВК — 0, 0, 2, 2 особи, что соответствовало ЛД50, равной 113,1 ± 8,9 мг/кг. Исходя из полученных значений ЛД50 оригинальных аминоэфиров вальпроевой кислоты соединения можно отнести к 3-му классу умеренно токсичных веществ.
На экспериментальной модели судорог, вызванных обратимым ингибитором ацетилхолиэстеразы (фенилкарбаматом) [12][13], установлено, что при введении АВК, ХАВК и ТАВК в двух дозах (21,5 и 43,0 мг/кг м.т.) доля погибших крыс статистически значимо не отличалась от группы животных, получавших судорожный агент, вне зависимости от дозы и регистрируемого временного промежутка. В ходе эксперимента была зарегистрирована гибель 1 животного в группе «Ф» на 30 мин наблюдения и гибель одной крысы при введении ТАВК в дозе 21,5 мг/кг м.т. на 10 мин наблюдения, а также гибель 3 крыс в группе ХАВК в дозе 43,0 мг/кг м.т. на 20 мин наблюдения.
После введения фенилкарбамата доля крыс с выраженными судорогами в группе «Ф» начинала снижаться с 30 мин наблюдения на 14%, и далее к 70 мин судороги у животных не регистрировали. Введение оригинальных аминоэфиров снижало количество животных с выраженностью судорог 4-го уровня и выше (шкала Racine), что соответствует генерализованному судорожному синдрому у человека (табл. 2).
При введении исследуемых субстанций в дозе 21,5 мг/кг м.т. статистически значимое уменьшение доли крыс с выраженными судорогами отмечали в период от 10 до 40 мин наблюдения (табл. 2). При этом в группе Ф+ХАВК животные с выраженными судорогами полностью отсутствовали начиная с 10 мин наблюдения, в то время как в двух других группах противосудорожный эффект наступил в более поздние сроки. Так, у животных в группе Ф+ТАВК на 10 мин выраженных судорог не наблюдали, однако в последующие 20 мин были зарегистрированы случаи клонико-тонических судорог, которые закончились к 40 мин, а в группе Ф+АВК снижение уровня судорог произошло уже к 20 мин наблюдения. Не выявлено статистически значимых межгрупповых различий при сравнении животных, получавших различные субстанции в одинаковый временной промежуток.
В случае введения субстанций в дозе 43,0 мг/кг м.т. противосудорожная эффективность в группах Ф+АВК и Ф+ТАВК в целом совпадала с установленной при меньшей дозе. Однако в группе Ф+ХАВК через 10 мин после введения субстанции количество животных с выраженными судорогами не снизилось по сравнению с группой «Ф». В то же время к 10 мин в группах Ф+АВК и Ф+ТАВК количество животных с судорожным синдромом было статистически значимо ниже, чем в группе с изолированным введением фенилкарбамата.
При оценке общей продолжительности судорог с применением статистической обработки результатов с использованием критерия Краскела – Уоллиса выявлено наличие статистически значимых различий между всеми исследуемыми группами при введении субстанций в обеих дозах (табл. 3).
В ходе анализа при построении квадратичной матрицы апостериорных сравнений (р-значения) продолжительности судорог после внутрибрюшинного введения исследуемых субстанций и в группе фенилкарбамата с использованием post-hoc теста по Данну не выявлено статистически значимых межгрупповых различий.
Наряду с этим при сравнении продолжительности судорог в группе Ф+ХАВК (доза 21,5 мг/кг м.т.) со значениями в группе «Ф» обнаружено статически значимое снижение Me продолжительности судорог на 77% (р = 0,001). Также зафиксирована меньшая Me продолжительности судорог на 57% при сравнении показателя в группах Ф+ХАВК и Ф+АВК на уровне дозы 21,5 мг/кг м.т. (р = 0,041).
При введении субстанций в дозе 43,0 мг/кг м.т. установлены различия во времени продолжительности судорог, сопоставимые с результатами, полученными при изучении эффектов введения меньшей дозы, а именно при сравнении показателя в группе Ф+ХАВК с группой фенилкарбамата (р = 0,001) и межгруппового различия Ф+ХАВК и Ф+АВК (р = 0,039).
Рассчитаны взвешенные по времени суммы баллов интенсивности судорог (AUC, площадь под кривой «судороги в баллах-время»). Погибшие особи из расчетов исключались. Продемонстрировано (табл. 4) наличие статистически значимых различий между показателями AUC при введении субстанций в дозах 21,5 мг/кг м.т. (р = 0,001) и 43,0 мг/кг м.т. (р = 0,001).
Установлено, что при введении субстанций в дозе 21,5 мг/кг м.т. взвешенные по времени суммы баллов интенсивности судорог в группе Ф+АВК были на 77% статистически значимо ниже, чем аналогичный показатель в группе фенилкарбамата (р = 0,041), а в группе Ф+ХАВК — на 93% (р = 0,001) по медиане соответственно. В группе Ф+ТАВК уровень AUC был ниже на 84%, однако не достигал уровня статистической значимости в сравнении с группой «Ф». Статистически значимое снижение показателя AUC зафиксировано также в группе Ф+ХАВК по сравнению с группой Ф+ТАВК, разница составила 78% (р = 0,026).
При введении субстанций в дозе 43,0 мг/кг м.т. отмечено достоверное снижение Ме показателя AUC в группе Ф+АВК на 59% (р = 0,015) и в группе Ф+ТАВК на 79% (р = 0,001) по сравнению с животными, получавшими фенилкарбамат.
На рисунках 1 и 2 представлена динамика медианных значений балльной оценки выраженности судорожного синдрома (от 0 до 6 баллов по шкале Racine) после введения исследуемых субстанций на протяжении 100 мин наблюдения. Введение субстанции ХАВК в дозе 21,5 мг/кг м.т. демонстрировало наиболее благоприятный график зависимости выраженности судорожного синдрома от времени, что соответствует большей противосудорожной эффективности данного соединения. В то время как при введении дозы 43,0 мг/кг м.т. более предпочтительные изменения наблюдали у животных, получивших АВК и ТАВК.
Таблица 1. Молекулярные характеристики аминоэфиров вальпроевой кислоты
Название | Брутто-формула | Чистота (%) |
(1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид (АВК) | С14Н27NO2*HCl | 98,27 |
1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат (ХАВК) | C15H27NO2*HCl | 98,03 |
8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпента-ноат (ТАВК) | C16H29NO2*HCl | 98,09 |
Таблица составлена авторами
Таблица 2. Влияние исследуемых лекарственных средств на возникновение судорог у крыс при введении фенилкарбамата и субстанций аминоэфиров вальпроевой кислоты
Группа | Временные промежутки, мин | ||||||||
0 | 5 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
Количество крыс (n/N) при введении субстанций в дозе 21,5 мг/кг м.т. | |||||||||
Ф | 8/8 | 8/8 | 8/8 | 8/8 | 6/7 | 5/7 | 3/7 | 1/7 | 0/7 |
Ф+АВК | 8/8 | 8/8 | 3/8* | 0/8* | 0/8* | 0/8* | 0/8 | 0/8 | 0/8 |
Ф+ТАВК | 8/8 | 8/8 | 0/7* | 3/7* | 1/7* | 0/7* | 0/7 | 0/7 | 0/7 |
Ф+ХАВК | 8/8 | 8/8 | 0/8* | 0/8* | 0/8* | 0/8* | 0/8 | 0/8 | 0/8 |
Количество крыс (n/N) при введении субстанций в дозе 43,0 мг/кг м.т. | |||||||||
Ф | 8/8 | 8/8 | 8/8 | 8/8 | 6/7 | 5/7 | 3/7 | 1/7 | 0/7 |
Ф+АВК | 8/8 | 8/8 | 2/8* | 0/8* | 0/8* | 0/8* | 0/8 | 0/8 | 0/8 |
Ф+ТАВК | 8/8 | 8/8 | 1/8* | 1/8* | 0/8* | 0/8* | 0/7 | 0/7 | 0/7 |
Ф+ХАВК | 8/8 | 8/8 | 8/8 | 0/8* | 0/8* | 0/8* | 0/8 | 0/8 | 0/8 |
Таблица составлена авторами по собственным данным
Примечания: Ф — фенилкарбамат; АВК — (1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид; ХАВК — 1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат; ТАВК — 8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпентаноат; n — количество крыс с выраженными судорогами; N — общее количество крыс в группе; * — различия статистически значимы в сравнении с группой Ф (р ≤ 0,05).
Таблица 3. Сравнительная оценка продолжительности судорог у крыс после внутрибрюшинного введения фенилкарбамата и субстанций аминоэфиров вальпроевой кислоты в дозах 21,5 и 43,0 мг/кг м.т.
Группа | Доза аминоэфиров вальпроевой кислоты | Количество животных | Продолжительность судорог, мин | р-значение межгрупповых различий1 | ||
N | Me | Min | Max | |||
Ф | – | 8 | 87,0 | 13,0 | 103,0 | 0,003 |
Ф+АВК | 21,5 мг/кг м.т. | 8 | 46,5 | 34,0 | 57,0 | |
Ф+ТАВК | 8 | 40,0 | 8,0 | 44,0 | ||
Ф+ХАВК | 8 | 20,0 | 20,0 | 20,0 | ||
Ф | – | 8 | 87,0 | 13,0 | 103,0 | 0,002 |
Ф+АВК | 43,0 мг/кг м.т. | 8 | 70,0 | 31,0 | 81,0 | |
Ф+ТАВК | 8 | 48,0 | 45,0 | 50,0 | ||
Ф+ХАВК | 8 | 30,0 | 12,0 | 32,0 | ||
Таблица составлена авторами по собственным данным
Примечание: Ф — фенилкарбамат; АВК — (1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид; ХАВК — 1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат; ТАВК — 8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпентаноат; «–» — изолированное введение фенилкарбамата; 1 – p-значение в критерии Краскела – Уоллиса.
Таблица 4. Сравнительная оценка взвешенной по времени суммы баллов интенсивности судорог у крыс самцов после внутрибрюшинного введения субстанций аминоэфиров вальпроевой кислоты в дозах 21,5 и 43,0 мг/кг м.т.
Группа | Доза аминоэфиров вальпроевой кислоты | Количество животных | Взвешенные по времени суммы баллов интенсивности судорог, баллы/мин | р-значение межгрупповых различий1 | ||
Me | min | max | ||||
Ф | – | 7 | 270 | 210 | 310 | 0,001 |
Ф+АВК | 21,5 мг/кг м.т. | 8 | 61 | 53 | 98 | |
Ф+ТАВК | 7 | 85 | 48 | 115 | ||
Ф+ХАВК | 8 | 19 | 18 | 20 | ||
Ф | – | 7 | 270 | 210 | 310 | 0,001 |
Ф+АВК | 43,0 мг/кг м.т. | 8 | 110 | 63 | 183 | |
Ф+ТАВК | 8 | 66 | 65 | 165 | ||
Ф+ХАВК | 5 | 78 | 78 | 90 | ||
Таблица составлена авторами по собственным данным
Примечание: Ф — фенилкарбамат; АВК — (1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид; ХАВК — 1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат; ТАВК — 8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпентаноат; «–» — изолированное введение фенилкарбамата; 1 – p-значение в критерии Краскела – Уоллиса.
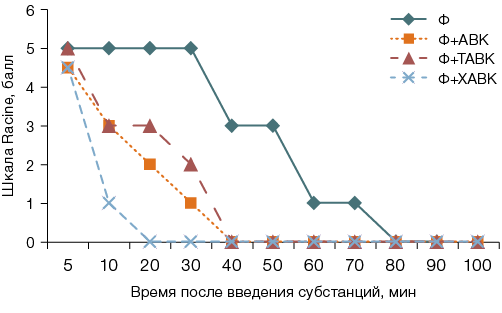
Рисунок подготовлен авторами по собственным данным
Рис. 1. Обобщенные по медиане графики зависимости выраженности судорожного синдрома по шкале Racine в баллах от времени после введения самцам крыс субстанций аминоэфиров вальпроевой кислоты в дозе 21,5 мг/кг м.т.: Ф — фенилкарбамат; АВК — (1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид; ХАВК — 1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат; ТАВК — 8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпентаноат
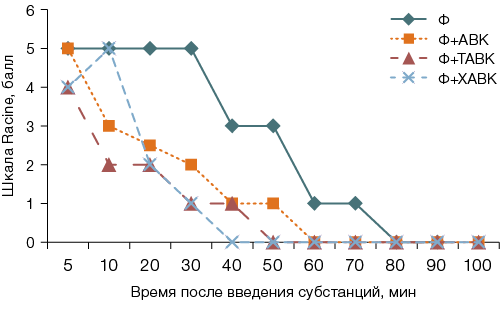
Рисунок подготовлен авторами по собственным данным
Рис. 2. Обобщенные по медиане графики зависимости выраженности судорожного синдрома по шкале Racine в баллах от времени после введения самцам крыс субстанций аминоэфиров вальпроевой кислоты в дозе 43 мг/кг м.т.: Ф — фенилкарбамат; АВК — (1-метилпиперидин-4-ил)-2-пропилпентаноата гидрохлорид; ХАВК — 1-азабицикло[ 2,2,2]oкт-3-ил-2-пропилпентаноат; ТАВК — 8-метил-8-азабицикло[ 3,2,1]окто-3-ил-2-пропилпентаноат
ОБСУЖДЕНИЕ
Полученные результаты свидетельствуют о том, что введение оригинальных аминоэфиров вальпроевой кислоты в организм на фоне острой интоксикации ингибитором холинэстераз способствовало выраженному снижению продолжительности судорог в первые 10–20 мин от начала воздействия. Наибольшую эффективность продемонстрировал ХАВК в дозе 21,5 мг/кг м.т.: через 10 мин судороги прекращались у 100% животных.
Стандартизированная по времени сумма баллов интенсивности судорог (AUC) в группах, получавших оригинальные аминоэфиры вальпроевой кислоты в обеих дозировках, была значительно ниже по сравнению с группой животных без терапии (только введение фенилкарбамата), что свидетельствует о хорошей эффективности исследуемых субстанций при снижении выраженности не только интенсивных, но и других видов судорог. В целом наименьшее значение медианного уровня AUC (соответственно, наибольшая эффективность) установлено для ХАВК (хинуклидинольный эфир вальпроевой кислоты) при введении в дозе 21,5 мг/кг м.т. Образцы АВК и ТАВК в изученных дозировках были сопоставимы друг с другом по эффективности.
Несмотря на то что статистически значимых различий между исследуемыми группами во всех временных промежутках при изучении летальности не обнаружено, выявленные случаи гибели трех животных на 20 мин эксперимента на фоне применения ХАВК в высокой дозе (43,0 мг/кг м.т.) требуют дальнейшего изучения. Очевидно, что эти случаи могут быть связаны как с токсичностью ХАВК, так и с индивидуальной реакцией отдельных особей на воздействие фенилкарбамата, вне зависимости от применения ХАВК. Кроме того, выраженная эффективность ХАВК в дозе 21,5 мг/кг м.т. позволяет предположить, что возможно дальнейшее снижение дозы без потери эффективности, а доза 43 мг/кг м.т. является избыточной. Ранее установлено, что противосудорожная эффективность вальпроамида в эксперименте на мышах в 3–5 раз выше, чем у вальпроевой кислоты [9], возможно, и в случае ХАВК оптимальная доза также будет значительно ниже и не будет связана с какими-либо проявлениями токсичности.
Поскольку ранее продемонстрировано, что введение АВК животным в эксперименте снижало продолжительность судорожного синдрома эффективнее, чем атропин, являющийся стандартным антидотом при интоксикации ингибиторами холинэстераз [17], разработанные оригинальные производные вальпроевой кислоты следует признать перспективными для дальнейшего изучения и разработки средств купирования судорожного синдрома ингибиторами холинэстераз, в том числе и необратимыми.
ВЫВОДЫ
- Разработанные оригинальные производные вальпроевой кислоты (АВК, ХАВК и ТАВК) эффективны при купировании судорожного синдрома, развивающегося на фоне отравления ингибитором холинэстеразы, и могут быть использованы для дальнейшего изучения в качестве лекарственных средств.
- По совокупности изученных параметров наибольшей противосудорожной эффективностью в дозе 21,5 мг/кг м.т. обладала субстанция ХАВК, однако при использовании дозы на уровне 43 мг/кг м.т. более эффективное купирование судорожного синдрома продемонстрировала субстанция АВК. Субстанция ТАВК проявляла свою противосудорожную эффективность при использовании повышенной дозы на уровне 43 мг/кг м.т.
- Необходимо провести дополнительный подбор эффективной дозы и изучить проявления токсичности хинуклидинольного эфира вальпроевой кислоты (ХАВК).
1 СП 2.2.1.3218-14 от 28.09.2014 «Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)».
2 Миронов АН. Руководство по проведению доклинических исследований лекарственных средств. Часть 1. М.: Гриф и К; 2012.
Список литературы
1. King AM, Aaron CK. Organophosphate and carbamate poisoning. Emergency Medicine Clinics of North America. 2015;33(1):133–51. https://doi.org/10.1016/j.emc.2014.09.010
2. Matošević A, Bosak A. Carbamate group as structural motif in drugs: a review of carbamate derivatives used as therapeutic agents. Arhiv za Higijenu Rada I Toksikologiju. 2020;71(4):285–99. https://doi.org/10.2478/aiht-2020-71-3466
3. Reddy BS, Skaria TG, Polepalli S, Vidyasagar S, Rao M, Vijayanarayana K, et al. Factors associated with outcomes in organophosphate and carbamate poisoning: a retrospective study. Toxicological Research. 2020;36(3):257–66. https://doi.org/10.1007/s43188-019-00029-x
4. Гладких ВД, Назаров ВБ. Реактиваторы холинэстеразы в терапии отравлений нейротропными физиологически активными веществами. Медицина экстремальных ситуаций. 2014;1(47):54–6. EDN: SAFQEV
5. Alozi M, Rawas-Qalaji M. Treating organophosphates poisoning: management challenges and potential solutions. Critical Reviews in Toxicology. 2020;50(9):764–79. https://doi.org/10.1080/10408444.2020.1837069
6. Reddy DS. Mechanism-based novel antidotes for organophosphate neurotoxicity. Current Opinion in Toxicology.2019;14:35–45. https://doi.org/10.1016/j.cotox.2019.08.001
7. Romoli M, Mazzocchetti P, D’Alonzo R, Siliquini S, Rinaldi VE, Verotti A, et al. Valproic Acid and Epilepsy: From Molecular Mechanisms to Clinical Evidences. Current Neuropharmacology. 2019;17(10):926–46 https://doi.org/10.2174/1570159X17666181227165722
8. Bialer M, Cross H, Hedrich UBS, Lagae L, Lerche H, Loddenkemper T. Novel treatment approaches and pediatric research networks in status epilepticus. Epilepsy & Behavior. 2019;101(Pt B):106564. https://doi.org/10.1016/j.yebeh.2019.106564
9. Delage C, Palayer M, Etain B, Hagenimana M, Blaise N, Smati J, et al. Valproate, divalproex, valpromide: Are the differences in indications justified? Biomedicine & Pharmacotherapy. 2023;158:114051. https://doi.org/10.1016/j.biopha.2022.114051
10. Mawasi H, Bibi D, Shekh-Ahmad T, Shaul C, Blotnik S, Bialer M. Pharmacokinetic-Pharmacodynamic Correlation and Brain Penetration of sec-Butylpropylacetamide, a New CNS Drug Possessing Unique Activity against Status Epilepticus. Molecular Pharmaceutics. 2016;13(7):2492–6. https://doi.org/10.1021/acs.molpharmaceut.6b00221
11. Haines KM, Matson LM, Dunn EN, Ardinger CE, LeeStubbs R, Bibi D, et al. Comparative efficacy of valnoctamide and sec-butylpropylacetamide (SPD) in terminating nerve agent-induced seizures in pediatric rats. Epilepsia. 2019;60(2):315–21 https://doi.org/10.1111/epi.14630
12. Прозоровский ВБ. Статистическая обработка результатов фармакологических исследований. Психофармакология и биологическая наркология. 2007;7(3–4):2090–120.
13. Прокопенко ЛИ, Зайцева МА, Беспалов АЯ, Мелехова АС, Петров АН, Бельская АВ и др. Гидрохлорид (1-метилпиперидин-4-ил)-2-пропилпентаноат, обладающий холинолитической и противосудорожной активностью. Патент Российской. Федерации № 2714135; 2020.
14. Беспалов АЯ, Прокопенко ЛИ, Горчакова ТЛ, Козлов ВК, Петров АН, Зайцева МА и др. Гидрохлориды замещенных 2-[(диметиламино)метил] арилдиметилкарбоматов, обладающие антихолинэстеразной активностью. Патент Российской. Федерации № 2754133; 2021.
15. Мелехова АС, Бельская АВ, Зорина ВН, Мельникова МВ, Кубарская ЛГ, Гайкова ОН. Новая экспериментальная модель судорожного синдрома на основе фенилкарбамата.
16. Racine RJ Modification of seizure activity by electrical stimulation. II. Motor seizure. Electroencephalography and Clinical Neurophysiology. 1972;32(3):281–94. https://doi.org/10.1016/0013-4694(72)90177-0
17. Мелехова АС, Петров АН, Беспалов АЯ, Бельская АВ, Мельникова МВ, Зацепин ЭП и др. Экспериментальная фармакотерапия судорожного синдрома при моделировании тяжелого отравления карбаматом. Medline.ru. Российский биомедицинский журнал. 2019;20(2):294–306.
Об авторах
А. В. БельскаяРоссия
Бельская Алиса Владимировна
Санкт-Петербург
А. С. Мелехова
Россия
Мелехова Александра Сергеевна
Санкт-Петербург
В. Н. Зорина
Россия
Зорина Вероника Николаевна - д-р биол. наук
Санкт-Петербург
А. Я. Беспалов
Россия
Беспалов Александр Яковлевич - канд. хим. наук
Санкт-Петербург
М. В. Мельникова
Россия
Мельникова Маргарита Викторовна
Санкт-Петербург
А. А. Бондаренко
Россия
Бондаренко Анастасия Александровна
Санкт-Петербург
Дополнительные файлы
Рецензия
Для цитирования:
Бельская А.В., Мелехова А.С., Зорина В.Н., Беспалов А.Я., Мельникова М.В., Бондаренко А.А. Противосудорожная активность оригинальных аминоэфиров вальпроевой кислоты при интоксикации ингибитором холинэстераз. Медицина экстремальных ситуаций. 2025;27(4):453-461. https://doi.org/10.47183/mes.2025-327
For citation:
Belskaya A.V., Melekhova A.S., Zorina V.N., Bespalov A.Ya., Melnikova M.V., Bondarenko A.A. Anticonvulsant activity of original valproic acid aminoethers in cholinesterase inhibitor poisoning. Extreme Medicine. 2025;27(4):453-461. https://doi.org/10.47183/mes.2025-327

















