Перейти к:
Применение модифицированного пакетирования в комплексном лечении обширных травматических повреждений печени
https://doi.org/10.47183/mes.2025-337
Аннотация
Введение. Травматические повреждения печени представляют собой серьезную проблему современной ургентной хирургии. Разработка новых методов хирургического гемостаза травматических повреждений печени является крайне актуальной задачей неотложной хирургии.
Цель. Разработка и апробация хирургического гемостаза при травматических повреждениях печени путем применения модифицированного пакетирования.
Материалы и методы. На кадаверном материале разработан новый метод хирургического гемостаза при травматических повреждениях печени. В клиническом исследовании приняли участие 27 пациентов с тяжелыми травматическими повреждениями печени (IV степень по AAST). Пациенты были разделены на две группы: основную (n = 14) и контрольную (n = 13). В лечении пациентов основной группы применен новый способ хирургического гемостаза травматических повреждений печени, заключающийся в тампонировании ран печени гемостатической марлей «Сургитамп», пропитанной гранулированным сорбентом «Молселект G-50», с последующим модифицированным пакетированием печени полосками полипропиленового сетчатого импланта; в контрольной группе хирургический гемостаз выполняли путем тампонирования раны печени гемостатическими губками с последующим ушиванием раны. Эффективность применения методики оценивали по следующим показателям: окончательный гемостаз, количество повторных кровотечений, количество повторных операций, летальность, длительность стационарного лечения, длительность пребывания в ОРИТ. Статистическую обработку результатов исследования проводили в программе Statistica 10.
Результаты. Применение модифицированного пакетирования в комплексном лечении пациентов с тяжелыми травматическими повреждениями печени позволило повысить надежность окончательного гемостаза с 46,2 до 92,8% (p = 0,0391), снизить количество повторных кровотечений и операций с 38,4 до 7,1% (p = 0,0391) и уменьшить уровень летальности с 38,4 до 14,2% (p > 0,05).
Выводы. Применение нового комбинированного метода хирургического гемостаза позволило улучшить результаты лечения пациентов с тяжелыми травматическими повреждениями печени за счет повышения надежности окончательного гемостаза, уменьшения повторных кровотечений и операций, снижения летальности.
Ключевые слова
Для цитирования:
Воронцов А.К., Пархисенко Ю.А., Чередников Е.Ф., Баранников С.В., Безалтынных А.А. Применение модифицированного пакетирования в комплексном лечении обширных травматических повреждений печени. Медицина экстремальных ситуаций. 2025;27(4):490-499. https://doi.org/10.47183/mes.2025-337
For citation:
Vorontsov A.K., Parhisenko Yu.A., Cherednikov E.F., Barannikov S.V., Bezaltynnykh A.A. Application of modified packing in the combination treatment of extensive traumatic liver injuries. Extreme Medicine. 2025;27(4):490-499. https://doi.org/10.47183/mes.2025-337
ВВЕДЕНИЕ
Травматические повреждения органов брюшной полости представляют собой серьезную проблему современной ургентной хирургии. По статистике травмы живота составляют от 1,5 до 36,5% из числа всех травматических повреждений. Однако частота летальных исходов при повреждениях органов брюшной полости достигает крайне высоких цифр — порядка 60%. При этом бóльшая часть пострадавших находится в молодом и трудоспособном возрасте, что определяет большую медико-социальную значимость проблемы травматических повреждений органов брюшной полости [1][2].
Особую группу повреждений при абдоминальной травме составляют повреждения паренхиматозных органов. Наиболее часто в клинической практике встречаются повреждения селезенки. Травмы печени в структуре повреждений паренхиматозных органов брюшной полости находятся на втором месте, однако представляют собой крайне сложную проблему для мировой хирургии. Тяжелые повреждения печени зачастую сопровождаются развитием трудноконтролируемого внутрибрюшного кровотечения и развитием печеночно-клеточной недостаточности в послеоперационном периоде при массивном размозжении печени, что является основными причинами неудовлетворительных результатов лечения пострадавших с травмой печени и высоких показателей летальности (до 50% и более) при данных повреждениях [3–5].
Большинство исследований последнего времени, касающихся проблемы травматических повреждений печени, направлены на совершенствование тактических подходов лечения травмы печени, применение технологий эндоваскулярного гемостаза и улучшение методов хирургического гемостаза повреждений печени [6].
Среди тактических подходов лечения тяжелых сочетанных повреждений все большее распространение получает стратегия этапного хирургического лечения «damage control surgery», направленная на сокращение первой фазы оперативного лечения с последующей стабилизацией состояния больного и проведением основного этапа хирургического лечения в более благоприятных условиях. Применение стратегии «damage control surgery» в настоящее время показывает хорошие результаты, однако не решает все проблемы хирургического лечения тяжелых травматических повреждений печени из-за развития ранних рецидивных кровотечений у пациентов с массивным повреждением печеночной паренхимы [7–9].
Важным современным достижением в лечении абдоминальной травмы, и прежде всего внутрибрюшных кровотечений, стало применение тактики консервативного лечения (Non-Operative Managementеt, NOM) [10][11]. Тактика NOM подразумевает проведение строгого отбора пациентов, оснащение стационаров рентген-эндоваскулярными операционными с обязательной системой динамического мониторинга за состоянием пациентов [12]. Однако большинство российских стационаров, оказывающих экстренную помощь пациентам с абдоминальной травмой, не имеют соответствующего оснащения, что ограничивает возможности применения тактики NOM в лечении пациентов с повреждениями печени [13].
На сегодняшний день основным методом лечения тяжелых травматических повреждений печени у пациентов с нестабильной гемодинамикой является экстренное оперативное вмешательство — срединная лапаротомия, главной задачей которой является надежная остановка внутрибрюшного кровотечения [14][15]. Разработаны и применяются в клинической практике множество способов гемостаза повреждений печени, как временных, так и окончательных, но ни один из них в настоящее время в полной мере не удовлетворяет хирургов из-за высокой частоты повторных кровотечений в послеоперационном периоде [16][17]. Разработка новых методов хирургического гемостаза травматических повреждений печени является крайне актуальной задачей современной ургентной хирургии [18].
Цель исследования — разработка и апробация хирургического гемостаза при травматических повреждениях печени путем применения модифицированного пакетирования.
МАТЕРИАЛЫ И МЕТОДЫ
Предварительно нами были проведены экспериментальные исследования по изучению возможности применения технологии хирургического гемостаза модифицированным пакетированием у лабораторных животных [19].
Также предварительно выполнены исследования на кадаверном материале с целью разработки методики оперативного вмешательства по применению модифицированного пакетирования. Исследования проведены на 7 нефиксированных трупах мужчин в возрасте 34,5 ± 3,2 года, умерших от причин, не связанных с травматическими повреждениями и заболеваниями органов брюшной полости, предоставленных бюджетным учреждением здравоохранения Воронежской области «Воронежское областное патологоанатомическое бюро». Разрешение на предоставление кадаверного материала соответствовало положениям действующего законодательства1. Временной промежуток от момента смерти до проведения исследования составил не более 24 ч.
На каждом объекте исследования моделировали травматическое повреждение печени. Для этого после проведения тотальной лапаротомии в рану выводили правую долю печени, которую помещали на подставку-столик.
На расстоянии 40 см от поверхности печени с помощью нити к лабораторному штативу крепили стальной груз массой 250 г. По готовности нить, фиксирующая груз, пережигалась пламенем газовой горелки, груз падал в вертикальном направлении и ударялся о диафрагмальную поверхность правой доли печени, что приводило к формированию раны печени (рис. 1А). Моделированную рану печени туго тампонировали гемостатической марлей «Сургитамп» (рис. 1Б), пропитанной гранулированным сорбентом «Молселект G-50» (рис. 1В), затем сдавливали правую долю печени марлевыми салфетками.
С целью проведения модифицированного пакетирования проводили мобилизацию правой доли печени. Для этого ножницами пересекали правую треугольную, венечную, серповидную и круглую связки печени, после чего правую долю печени выводили в рану. Затем полоску (шириной 4,0 см и длиной 30,0 см) из сетчатого полипропиленового импланта, используемого для пластики грыж, фиксировали в сагиттальной плоскости. Для этого край полоски сетчатого импланта подшивали к диафрагме тремя отдельными узловыми швами полипропиленовой мононитью (рис. 1Г). Далее обертывали диафрагмальную поверхность печени с переходом на висцеральную поверхность, сетчатый имплант натягивали для обеспечения компрессии и его нижний край фиксировали узловыми швами к краю начала полоски, создавая компрессию и натяжение. Важно проводить модифицированное пакетирование, отступив от краев желчного пузыря на 1,0–1,5 см, в дальнейшем его окутывали большим сальником (рис. 1Д).
С целью обеспечения дополнительной компрессии в поперечном направлении относительно правой доли печени подшивали три дополнительные полипропиленовые сетчатые полоски (рис. 1Е). Полоски окутывали большим сальником, фиксировали его отдельными узловыми швами к капсуле печени для профилактики возникновения кишечных свищей.
Следующим этапом исследования была клиническая апробация применения технологии модифицированного пакетирования у пострадавших с повреждениями печени. Пилотное рандомизированное контролируемое клиническое исследование проведено на базе Брянской городской больницы № 1, Воронежской областной клинической больницы № 1, Воронежской городской клинической больницы скорой медицинской помощи № 1, Воронежской городской клинической больницы скорой медицинской помощи № 10. В исследовании приняли участие 27 пострадавших с травматическим повреждением печени. Дизайн клинического исследования представлен на рисунке 2.
Критерии включения пациентов в исследование: закрытая травма живота; возраст пострадавших 18–80 лет; подписанное информированное согласие на участие в клиническом исследовании; степень повреждения печени согласно классификации американского общества хирургов и травматологов (American Association for the Surgery of Trauma, AAST) — IV [19]. Критерии невключения пациентов в исследование: отказ от участия в клиническом исследовании; агональное состояние пациента; аллергические реакции на «Молселект G-50», «Сургитамп» и полипропиленовый сетчатый имплант. Критерии исключения пациентов из исследования: отказ от продолжения участия в клиническом исследовании; повреждение полых органов, перитонит; повреждение печени I–III степени по AAST; множественные повреждения органов брюшной полости; макроскопические признаки цирроза печени; количество баллов по шкале военно-полевой хирургии для определения хирургической тактики > 13 баллов.
В зависимости от целей и задач исследования пациенты были разделены на две группы: основную (14 пациентов) и контрольную (13 пациентов). Распределение больных производили методом случайной выборки с использованием генератора случайных чисел. Больные были сопоставимы по полу, возрасту, характеру травматического повреждения печени, структуре сочетанных повреждений и тяжести кровопотери.
В основной группе пациентов для хирургического гемостаза травматических повреждений печени применяли метод, представленный в патенте [20]. В контрольной группе применялся метод хирургического гемостаза ран печени путем тампонирования ран печени гемостатическими коллагеновыми губками с последующим ушиванием раны печени мононитью ПГА 2,0.
В комплексном лечении больные обеих групп в послеоперационном периоде использовали стандартное консервативное лечение, включающее гемостатическую и инфузионную терапии, гемотрансфузии по показаниям, антибактериальную терапию, анальгетики и перевязки.
Результаты исследования оценивали по показателям окончательного гемостаза, количеству повторных кровотечений и повторных операций, времени оперативного вмешательства, длительности пребывания в отделении реанимации и интенсивной терапии, длительности стационарного лечения, летальности, наличию и характеру осложнений в послеоперационном периоде.
Статистическую обработку результатов исследования проводили в программе Statistica 10. Вычисляли стандартные описательные статистики (среднее значение (M), стандартную ошибку среднего значения (m), медиану (Me), нижний (Q1) и верхний (Q3) квартили). Для оценки нормальности распределения количественных показателей использовали критерий Шапиро – Уилка. Значимость различий количественных признаков в независимых группах определяли с использованием t-критерия Стьюдента (при нормальном распределении признака) и U-критерия Манна – Уитни (при распределении отличном от нормального). Анализ качественных признаков проводили с использованием критериев Фишера и Z-критерия с поправкой Йейтса. Различия признаков считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Общая характеристика пациентов, принявших участие в исследовании, представлена в таблице 1.
В таблице 1 представлены сводные данные о группах пациентов. Так, наиболее часто травматические повреждения печени встречались у мужчин трудоспособного возраста (20 (74,1%)). У женщин травматические повреждения встречались значительно реже: у 7 (25,9%) пострадавших. Средний возраст пациентов с травматическими повреждениями печени составил 36 [ 30; 43] лет. Анализируя механизм абдоминальной травмы, следует отметить, что среди причин травматических повреждений печени преобладали дорожно-транспортные происшествия (12 (44,5%) пациентов), реже встречалась кататравма (падение с высоты) (9 (22,2%) пациентов) и бытовая травма (6 (22,2%) пациентов).
Среди сочетанных повреждений наиболее часто встречались повреждения грудной клетки 17 (32,5%), реже — скелетная травма 9 (8,5%), черепно-мозговая травма 8 (59,0%) и повреждение таза 5 (18,5%).
При анализе сопутствующей патологии установлено, что пациенты с абдоминальной травмой и повреждениями печени были практически соматически здоровы. Лишь у 4 (14,8%) пациентов была выявлена сопутствующая патология: у 1 (3,7%) пациента — ишемическая болезнь сердца, у 3 (11,1%) пострадавших — хронический панкреатит.
В комплексном лечении пациентов основной группы был применен новый комбинированный метод хирургического гемостаза травматических повреждений печени, заключающейся в тампонировании ран печени гемостатической марлей «Сургитамп», пропитанной гранулированным сорбентом «Молселект G-50», с последующим модифицированным пакетированием печени полосками полипропиленового сетчатого импланта [20] (рис. 3А–Е).
В работе установлено, что сразу после тампонирования раны печени гемостатической марлей «Сургитамп», пропитанной гранулированным сорбентом «Молселект G-50», набухающим при контакте с кровью и увеличивающимся в объеме, он превращался в пропитанный кровью гидрогель. Гемостатическая марля «Сургитамп» обеспечивала компрессию и усиление гемостатического эффекта. Сдавление печени руками приводило к временному гемостазу. Однако при ослаблении компрессии кровотечение возобновлялось.
С целью достижения окончательного гемостаза применяли метод модифицированного пакетирования полосками полипропиленового сетчатого импланта (технология фиксации сетчатого импланта описана выше), что приводило к окончательной остановке кровотечения. Окончательный гемостаз в основной группе был достигнут у 13 (92,8%) пациентов. У 1 (7,14%) пациента основной группы на 2 сут после операции наблюдали признаки возобновления кровотечения. Пациент в экстренном порядке был оперирован. При ревизии органов брюшной полости установлен источник кровотечения — диффузное подтекание крови из раны печени за счет недостаточной компрессии при натяжении полосок полипропиленового сетчатого импланта. Дополнительное натяжение полосок привело к остановке кровотечения и окончательному гемостазу.
В основной группе умерло 2 (14,3%) пациента. Причиной летальных исходов явилась тяжелая сочетанная травма. По данным судебно-медицинского вскрытия, признаков повторного внутрибрюшного кровотечения в обоих случаях не наблюдалось.
В контрольной группе с целью достижения окончательного гемостаза повреждений печени рана тампонировалась гемостатическими коллагеновыми губками. Губки активно пропитывались кровью, однако диффузное кровотечение из ран печени сохранялось. Для достижения окончательного гемостаза раны печени ушивались П-образным швом (мононитью ПГА 2.0) до сближения краев раны. При прошивании ран печени наблюдали диффузное подтекание крови из мест вколов иглы, паренхима печени прорезалась шовным материалом, что затрудняло достижение окончательного гемостаза и удлиняло время проведения оперативного вмешательства. У 5 (38,4%) пациентов контрольной группы на 2–3 сут после операции наблюдали признаки повторного кровотечения. Больные были оперированы в экстренном порядке. Источником кровотечения во всех случаях было подтекание крови из разрывов печени. В контрольной группе умерли 5 (38,4%) пациентов на фоне острой кровопотери, постгеморрагической анемии, а также сочетанных повреждений.
Сравнительная эффективность применения модифицированного пакетирования в лечении травматических повреждений печени представлена в таблице 2.
Применение модифицированного пакетирования в комплексном лечении пациентов с тяжелыми травматическими повреждениями печени (класс IV по AAST) позволило повысить надежность окончательного гемостаза с 46,2 до 92,8% (p = 0,0391), снизить количество повторных кровотечений и операций с 38,4 до 7,1% (p = 0,0391) и уменьшить летальность с 38,4 до 14,2% (p > 0,05).
Анализ послеоперационных хирургических осложнений в группах исследования показал, что в послеоперационном периоде у 1 пациента основной группы было повторное кровотечение. Пациент в экстренном порядке был оперирован. При ревизии органов брюшной полости источником кровотечения оказалось диффузное подтекание крови из раны печени за счет недостаточной компрессии при натяжении полосок полипропиленового сетчатого импланта. Дополнительное натяжение полосок привело к остановке кровотечения и окончательному гемостазу.
В контрольной группе у 5 пациентов в послеоперационном периоде отмечали признаки повторного кровотечения. Пациенты были повторно оперированы. Интраоперационно выявлено прорезывание швов паренхимы печени, выполнен дополнительный гемостаз в объеме электрокоагуляции, нанесением на место диффузного подтекания крови пластины Тахокомба или дополнительным прошиванием мест разрывов. У одного пациента контрольной группы в послеоперационном периоде появились жалобы на боли в правом подреберье, слабость, было выполнено УЗИ брюшной полости, выявлена билома брюшной полости. Последнее осложнение потребовало пункционного дренирующего вмешательства под контролем УЗИ. Исход — полное разрешение, пациент выписан в удовлетворительном состоянии на амбулаторный этап на 18 сутки. У одного пациента в послеоперационном периоде на фоне острой массивной кровопотери развился ДВС-синдром, который потребовал интенсивной терапии в условиях ОРИТ; данное осложнение разрешилось.
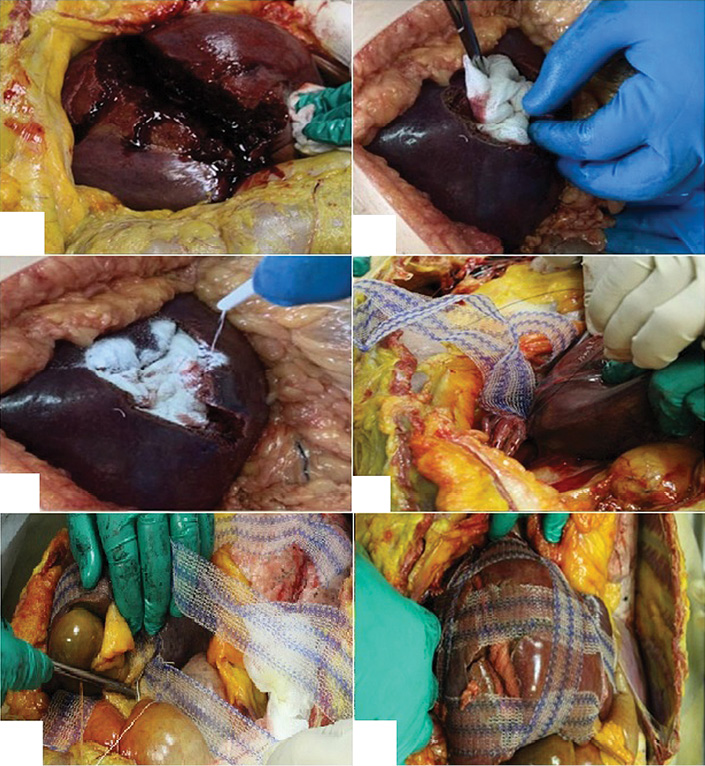
Фотографии предоставлены авторами
Рис. 1. Этапы модифицированного пакетирования печени на кадаверном материале: А — моделированная ушибленная рана правой доли печени; Б — тампонирование раны печени гемостатическим материалом «Сургитамп»; В — нанесение гранулированного сорбента «Молселект G-50»; Г — фиксация полосок полипропиленового сетчатого импланта к диафрагме; Д — фиксация полосок сетчатого импланта по висцеральной поверхности печени; Е — окончательный вид печени после модифицированного пакетирования
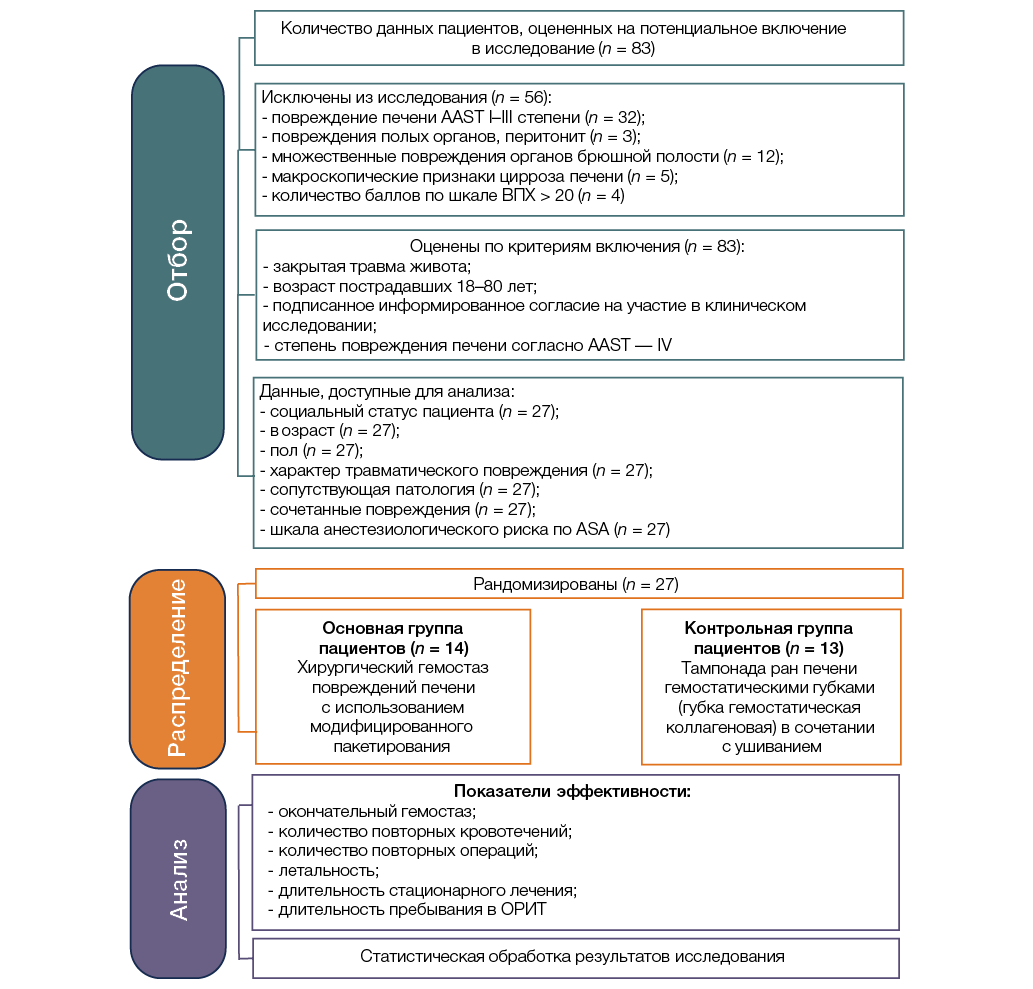
Рисунок подготовлен авторами
Рис. 2. Дизайн клинического исследования: ASA — Американское общество анестезиологов; ВПХ-шкала — шкалы объективной оценки тяжести повреждений, разработанные на кафедре военно-полевой хирургии Военно-медицинской академии; ОРИТ — отделение реанимации и интенсивной терапии,AAST — Американское общество хирургов и травматологов
Таблица 1. Характеристика групп исследования
Показатель | Основная группа (n = 14) | Контрольная группа (n = 13) | Уровень статистической значимости, p |
Работающие, n (%) | 3 (21,4%) | 5 (38,5%) | >0,05 |
Неработающие, n (%) | 8 (57,2%) | 8 (61,5%) | >0,05 |
Пенсионеры, n (%) | 3 (21,4%) | 0 | нд |
Возраст, годы Me [Q1; Q3] | 40 [ 54,0; 79.0] | 36,7 [ 37,0; 61,0] | >0,05 |
Мужчины, n (%) | 10 (58,7%) | 10 (78,2%) | >0,05 |
Женщины, n (%) | 4 (41,3%) | 3 (21,8%) | >0,05 |
Автодорожная травма, n (%) | 5 (35,7%) | 7 (53,8%) | >0,05 |
Падение с высоты, n (%) | 5 (21,4%) | 4 (23,1%) | >0,05 |
Бытовая травма, n (%) | 4 (28,6%) | 2 (15,4%) | >0,05 |
Ишемическая болезнь сердца, n (%) | 1 (83,2%) | 0 | нд |
Хронический панкреатит, n (%) | 1 (8,4%) | 2 (9,0%) | >0,05 |
Черепно-мозговая травма, n (%) | 4 (60,5%) | 4 (50,0%) | >0,05 |
Повреждения грудной клетки, n (%) | 9 (30,9%) | 8 (41,6%) | >0,05 |
Скелетная травма, n (%) | 5 (8,6%) | 4 (8,4%) | >0,05 |
Повреждение костей таза, n (%) | 3 (21,4%) | 2 (15,3%) | >0,05 |
II, n (%) | 5 (35,7%) | 4 (30,8%) | >0,05 |
III, n (%) | 7 (50%) | 8 (61,5%) | >0,05 |
IV, n (%) | 2 (14,3%) | 1 (7,7%) | >0,05 |
III, n (%) | 4 (28,6%) | 3 (23,2%) | >0,05 |
IV, n (%) | 6 (42,8%) | 5 (38,4%) | >0,05 |
V, n (%) | 4 (28,6%) | 5 (38,4%) | >0,05 |
Таблица составлена авторами по собственным данным
Примечание: нд — недостаточно данных; n — количество пациентов в группе.
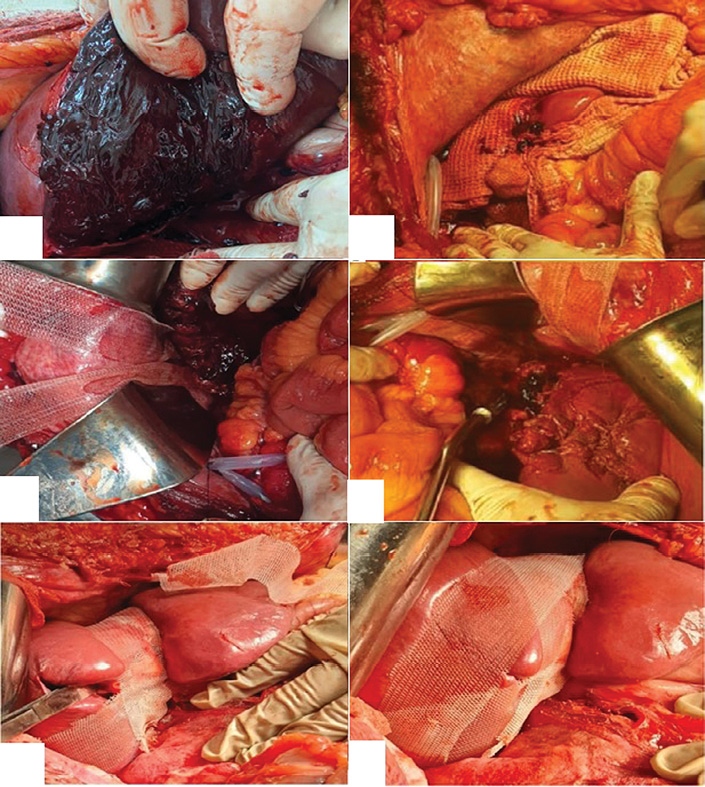
Фотографии предоставлены авторами
Рис. 3. Этапы выполнения модифицированного пакетирования у пациента с повреждением печени: А — внешний вид травматического разрыва V, VI, VII сегментов правой доли печени (AAST IV); Б — тампонирование раны гемостатическим материалом «Сургитамп», пропитанного гранулированным cорбентом «Молселект G-50», временная тампонада марлевым полотенцем; В — фиксация полосок полипропиленового импланта к диафрагме; Г, Д — фиксация полосок сетчатого импланта в поперечном направлении; Е — окончательный вид операционной раны
Таблица 2. Сравнительная эффективность лечения пациентов с травматическими повреждениями печени
Показатель | Основная группа (n = 14) | Контрольная группа (n = 13) | Уровень статистической значимости, p |
Окончательный гемостаз, n (%) | 13 (92,8%) | 6 (46,2%) | 0,0391 |
Повторные кровотечения, n (%) | 1 (7,1%) | 5 (38,4%) | 0,0391 |
Повторные операции, n (%) | 1 (7,1%) | 5 (38,4%) | 0,0391 |
Летальность, n (%) | 2 (14,2%) | 5 (38,4%) | >0,05 |
Медиана длительности стационарного лечения, койко-дни | 10,0 [ 9,0; 14,0] | 16,0 [ 10,0; 18,0] | >0,05 |
Медиана времени оперативного вмешательства, мин | 100,0 [ 85,0; 120,0] | 130,0 [ 120,0; 150,0] | 0,0022 |
Медиана длительности пребывания в ОРИТ, койко-дни | 3,0 [ 1,0; 4,0] | 5,0 [ 3,0; 6,0] | 0,011 |
Медиана объема трансфузии эритроцитарной взвеси, мл | 1140 [ 1100; 1200] | 1230 [ 1150; 1900] | 0,0272 |
Медиана объема трансфузии СЗП, мл | 1175 [ 1100; 1250] | 1430 [ 1350; 2100] | 0,0001 |
Послеоперационные осложнения (по Clavien–Dindo) | |||
III, n (%) | 1 (7,1%) | 5 (38,4%) | >0,05 |
IIIa, n (%) | – | 1 (7,7%) | нд |
IV, n (%) | – | 1 (7,7%) | нд |
V, n (%) | 2 (14,2%) | 5 (38,4%) | >0,05 |
Таблица составлена авторами по собственным данным
Примечание: нд — недостаточно данных; n — количество пациентов в группе.
ОБСУЖДЕНИЕ
Повреждения органов брюшной полости представляют собой одну из наиболее сложных и во многом не решенных проблем неотложной хирургии [5][9]. В структуре травматизма при абдоминальной травме повреждения печени находятся на втором месте, уступая лишь повреждениям селезенки. Однако наиболее высокие показатели летальности (14–58%) у пациентов с закрытой травмой живота приходятся именно на тяжелые повреждения печени, что обусловлено массивным внутрибрюшным трудноконтролируемым кровотечением и развитием печеночно-клеточной недостаточности в послеоперационном периоде [13][18].
Самой частой причиной летальных исходов при абдоминальной травме являются травматические разрывы печени, осложненные массивным кровотечением. В таких случаях основное значение имеют два фактора: своевременность и быстрота проведения оперативного вмешательства и применение надежного эффективного способа хирургического гемостаза [6].
Большинство хирургов в экстренных случаях применяют ушивание ран, электрокоагуляцию, тампонирование. Существенным недостатком при этом считается появление ишемических зон некроза между швами. При глубоких повреждениях используют тампонирование ран сальником, различными гемостатическими губками, пленками, порошкообразными гемостатиками. Но, как показывает практика, они оказываются малоэффективными. Тампонада глубоких ран полотенцем, салфеткой или любым нерассасывающимся материалом вызывает необходимость проведения повторных операций [3].
При обширных травматических повреждениях печени эффективным способом остановки кровотечения является пакетирование разрывов печени полипропиленовым сетчатым имплантом. При этом производится мобилизация печени от всех связок с обязательным сохранением оттока крови по венам. Но в послеоперационном периоде после стабилизации состояния всех пациентов необходимо повторно оперировать для проведения окончательного хирургического пособия [1].
Приведенные данные свидетельствуют, что существует множество способов гемостаза при повреждениях печени, но ни один из них не удовлетворяет хирургов. В этой связи разработка новых способов хирургического гемостаза травматических повреждений печени является актуальной проблемой ургентной хирургии.
Перед началом клинического исследования нами были проведены многофункциональные интегрированные морфологические, морфометрические, иммуногистохимические исследования на лабораторных животных по разработке нового способа хирургического гемостаза [3]. В серии экспериментов in vivo изначально было показано, что применение гемостатика «Сургитамп» и сорбента «Молселект G-50» эффективно останавливает умеренное паренхиматозное кровотечение на моделях кровоточащих ран печени, а в эксперименте на моделях с активным кровотечением из ран печени разработанная методика комбинированного хирургического гемостаза с применением гемостатических средств и модифицированного пакетирования показала высокую эффективность местного гемостаза [19].
В соответствии с целью нашего клинического исследования разработанный новый способ хирургического гемостаза с модифицированным пакетированием [20] был применен у самой тяжелой категории пациентов с травматическим повреждением печени, осложненным активным кровотечением (IV степени по AAST).
ЗАКЛЮЧЕНИЕ
Разработан и внедрен в клиническую практику новый метод хирургического гемостаза, реализующийся путем тампонирования ран печени гемостатической марлей «Сургитамп», пропитанной гранулированным сорбентом «Молселект G-50», с последующим модифицированным пакетированием печени полосками полипропиленового сетчатого эндопротеза. Это позволило улучшить результаты лечения пациентов с тяжелыми травматическими повреждениями печени за счет повышения надежности окончательного гемостаза, уменьшения повторных кровотечений и операций, снижения уровня летальности.
1 Постановление Правительства Российской Федерации № 750 «Об утверждении Правил передачи невостребованного тела, органов и тканей умершего человека для использования в медицинских, научных и учебных целях, а также использования невостребованного тела, органов и тканей умершего человека в указанных целях» (с изменениями и дополнениями) от 21.07.2012.
Список литературы
1. García IC, Villalba JS, Iovino D, Franchi C, Iori V, Pettinato G, et al. Liver Trauma: Until When We Have to Delay Surgery? A Review. Life. 2022;12(5):694. https://doi.org/10.3390/life12050694
2. Corvino F, Giurazza F, Marra P, Ierardi AM, Corvino A, Basile A, et al. Damage Control Interventional Radiology in Liver Trauma: A Comprehensive Review. Journal of Personalized Medicine. 2024;14(4):365. https://doi.org/10.3390/jpm14040365
3. Воронцов АК, Пархисенко ЮА, Чередников ЕФ, Баранников СВ, Черных АВ, Безалтынных АА и др. Экспериментальное обоснование применения нового метода хирургического гемостаза обширных травматических повреждений печени. Волгоградский научно-медицинский журнал. 2023;20(2):45–50. EDN: HSJMKR
4. Евтихов АВ, Любивый ЕД, Ким ВЛ. Клинические наблюдения тяжелых травматических повреждений печени. Хирургия. Журнал им. Н.И. Пирогова. 2020;7:89–92. https://doi.org/10.17116/hirurgia202007189
5. Александров ВВ, Маскин СС, Алимов МН, Бирюлев ДС, Матюхин ВВ, Рашид А и др. Закрытая травма печени. Систематический обзор. Журнал им. Н.В. Склифосовского «Неотложная медицинская помощь». 2025;14(1):141–54. https://doi.org/10.23934/2223-9022-2025-14-1-141-154
6. Coccolini F, Coimbra R, Ordonez C, Kluger Y, Vega F, Moore EE, et al. Liver trauma: WSES 2020 guidelines. World Journal of Emergency Surgery. 2020;15(1):24. https://doi.org/10.1186/s13017-020-00302-7
7. Benz D, Balogh ZJ. Damage control surgery: current state and future directions. Current Opinion in Critical Care. 2017;23(6):491–7. https://doi.org/10.1097/mcc.0000000000000465
8. Ordoñez CA, Parra MW, Millán M, Caicedo Y, GuzmanRodriguez M, Padilla N, et al. Damage Control in Penetrating Liver Trauma: Fear of the Unknown. Colombia Médica. 2020;51(4):e4134365.
9. Чубарян КА, Грошилин ЮВ, Лукаш ВС. Возможности улучшения результатов хирургического лечения пациентов с тяжелыми травмами печени. Политравма. 2024;3:19–27. https://doi.org/10.24412/1819-1495-2024-3-19-27
10. Brooks A, Reilly JJ, Hope C, Navarro A, Naess PA, Gaarder C. Evolution of non-operative management of liver trauma. Trauma Surgery and Acute Care Open. 2020;5(1):e000551. https://doi.org/10.1136/tsaco-2020-000551
11. Iacobellis F, Di Serafino M, Caruso M, Dell’Aversano Orabona G, Rinaldo C, Grimaldi D, et al. Non-Operative Management of Polytraumatized Patients: Body Imaging beyond CT. Diagnostics. 2023;13(7):1347. https://doi.org/10.3390/diagnostics13071347
12. Александров ВВ, Маскин СС, Ермолаева НК, Матюхин ВВ. Консервативное ведение пациентов с закрытой травмой паренхиматозных органов брюшной полости и забрюшинного пространства, с забрюшинными кровоизлияниями — показания, методика и целесообразность. Журнал им. Н.В. Склифосовского «Неотложная медицинская помощь». 2021;3:540–7. https://doi.org/10.23934/2223-9022-2021-10-3-540-548
13. Гаврищук ЯВ, Мануковский ВА, Тулупов АН, Демко АЕ, Колчанов ЕА, Савелло ВЕ и др. Диагностика и лечение повреждений печени при закрытой травме живота с использованием малоинвазивных технологий. Вестник хирургии им. И.И. Грекова. 2022;181(3):28–36. https://doi.org/10.24884/0042-4625-2022-181-3-28-36
14. Подолужный ВИ, Радионов ИА, Пельц ВА, Старцев АБ, Краснов КА, Шаталин ВА. Травматическое повреждение печени. Политравма.2023;1:34–8. https://doi.org/10.24412/1819-1495-2023-1-34-38
15. Липатов ВА, Лазаренко СВ, Северинов ДА, Денисов АА, Чупахин ЕГ, Анискина ЕН. Сравнительный анализ эффективности новых образцов местных гемостатических средств. Медицина экстремальных ситуаций. 2023;25(4):131–6. https://doi.org/10.47183/mes.2023.063
16. Баранников СВ, Чередников ЕФ, Полубкова ГВ, Банин ИН, Болховитинов АЕ, Бережной СИ и др. Применение альгинатного полимерного полисахаридного гемостатического гидрогеля при продолжающемся артериальном кровотечении из пептической язвы гастроэнтероанастомоза (клинический случай). Медицина экстремальных ситуаций. 2025;27(2):235–42. https://doi.org/10.47183/mes.2025-243
17. Гаврищук ЯВ, Мануковский ВА, Тулупов АН, Демко АЕ, Колчанов ЕА, Киселев МА и др. Лечение пострадавшей с закрытой травмой печени с использованием интервеционных методов. Вестник экспериментальной и клинической хирургии. 2023;16(4):316–20. https://doi.org/10.18499/2070-478X-2023-16-4-316-320
18. Tinkoff G, Esposito TJ, Reed J, Kilgo P, Fildes J, Pasquale M, et al. American Association for the Surgery of Trauma Organ Injury Scale I: spleen, liver, and kidney, validation based on the National Trauma Data Bank. Journal of the American College of Surgeons. 2008;207(5):646–55. https://doi.org/10.1016/j.jamcollsurg.2008.06.342
19. Воронцов АК, Пархисенко ЮА, Чередников ЕФ, Баранников СВ, Безалтынных АА, Черных АВ. Использование гемостатической марли Сургитамп и гранулированного сорбента Молселект G-50 и в лечении экспериментальных кровоточащих ран печени. Вестник экспериментальной и клинической хирургии. 2023;1(16):52–9. https://doi.org/10.18499/2070-478X-2023-16-1-52-59
20. Воронцов АК, Пархисенко ЮА, Воронцов КЕ, Безалтынных АА. Способ хирургического лечения больных с тяжелыми травмами печени. Патент Российской Федерации № 2674874 С1; 2018. EDN: ZECXBR
Об авторах
А. К. ВоронцовРоссия
Воронцов Алексей Константинович - канд. мед. наук
Смоленск
Ю. А. Пархисенко
Россия
Пархисенко Юрий Александрович - д-р мед. наук
Воронеж
Е. Ф. Чередников
Россия
Чередников Евгений Федорович - д-р мед. наук
Воронеж
С. В. Баранников
Россия
Баранников Сергей Викторович - канд. мед. наук
Воронеж
А. А. Безалтынных
Россия
Безалтынных Александр Александрович - д-р мед. наук
Смоленск
Дополнительные файлы
Рецензия
Для цитирования:
Воронцов А.К., Пархисенко Ю.А., Чередников Е.Ф., Баранников С.В., Безалтынных А.А. Применение модифицированного пакетирования в комплексном лечении обширных травматических повреждений печени. Медицина экстремальных ситуаций. 2025;27(4):490-499. https://doi.org/10.47183/mes.2025-337
For citation:
Vorontsov A.K., Parhisenko Yu.A., Cherednikov E.F., Barannikov S.V., Bezaltynnykh A.A. Application of modified packing in the combination treatment of extensive traumatic liver injuries. Extreme Medicine. 2025;27(4):490-499. https://doi.org/10.47183/mes.2025-337

















